O diabetes mellitus tipo 1 (DM1) é a doença endocrinometabólica crônica mais comum na infância e adolescência e a terceira doença crônica mais prevalente em crianças1,2. Caracteriza-se pela destruição das células beta-pancreáticas e consequente redução da produção de insulina3. Subdivide-se em DM1 tipo 1A (imunomediada) e 1B (idiopática); estando a primeira associada a presença de autoanticorpos, como os anti-ilhota (ICA), antidescarboxilase do ácido glutâmico (anti-GAD), antitirosina fosfatase (IA-2A), anti-insulina (IAA) e antitransportador de zinco 8 (anti-ZnT8)4.
O processo imunológico que se desenvolve progressivamente nas células beta-pancreáticas destes indivíduos é capaz de afetar outros órgãos, resultando no surgimento de novas doenças autoimunes, tornando-as mais frequentes entre pacientes diabéticos quando em comparação com a população pediátrica geral5. Aquelas com maior prevalência são a tireoidite de Hashimoto e a doença de Graves (15-30%), denominadas em conjunto neste estudo como doença tireoidiana autoimune (DTAI), seguidas pela doença celíaca (1-16%), gastrite autoimune/anemia perniciosa (5-10%), vitiligo (2-10%) e doença de Addison (0,5%)6.
Considerando as bases fisiopatológicas da autoimunidade e o prejuízo ao controle glicêmico e lipídico que pode resultar da coexistência do DM1 e de outras DAI, este estudo objetivou avaliar a prevalência de marcadores autoimunes associados às células beta-pancreáticas, tireoidites e doença celíaca em crianças e adolescentes com DM1 ao diagnóstico e durante seu seguimento clínico. De modo secundário, objetivou estabelecer associações entre características clínicas e demográficas dos pacientes e a autoimunidade, além de associações de predisposição entre as doenças a partir da presença de determinados anticorpos.
MÉTODO
Realizou-se um estudo observacional, longitudinal, com coleta de dados retrospectiva por meio da revisão de prontuários de crianças e adolescentes atendidos em ambulatório de Endocrinologia Pediátrica ou admitidos nas Unidades de Internação Pediátrica de um hospital terciário localizado em Curitiba-PR.
Como critérios de inclusão, foram considerados os pacientes com idade inferior a 16 anos atendidos em primeira consulta no ambulatório de diabetes da Unidade de Endocrinologia Pediátrica ou admitidos nas Unidades de Internação do Departamento de Pediatria da instituição no período de janeiro de 2014 a dezembro de 2016. Foram excluídos os pacientes com registros em prontuário incompletos ou inconclusivos.
As variáveis estudadas incluíram: a) características sociodemográficas (idade atual e ao diagnóstico de DM1; sexo; procedência); b) características clínicas (presença de fatores de estresse emocional relacionados ao diagnóstico de DM1; presença de doenças autoimunes associadas no momento do diagnóstico e a sua evolução durante o acompanhamento clínico; história mórbida pregressa e familiar dos pacientes); características laboratoriais (valores gasométricos de pH e bicarbonato; presença de cetoacidose e sua gravidade ao diagnóstico; exames de função tireoidiana – TSH e T4 livre; análise da presença de autoanticorpos pancreáticos – anti-GAD, ICA, IA-2A e IAA, autoanticorpos tireoidianos – anticorpo antitireoperoxidase (anti-TPO) e anticorpo antitireoglobulina (anti-TG), autoanticorpos relacionados a doença celíaca – anticorpo antiendomísio (anti-EMA) e anticorpo antitransglutaminase tecidual (anti-tTG), níveis séricos de imunoglobulina A (IgA) total.
A história familiar de doença autoimune (DAI) foi considerada positiva somente quando houve relato de histórico conhecido de DAI em familiares de primeiro ou segundo graus (pais, irmãos, avós). A presença de cetoacidose ao diagnóstico e a classificação de sua gravidade foram definidas segundo critérios da ISPAD7, sendo leve quando pH < 7,3 ou bicarbonato < 15mmol/L; moderada quando pH < 7,2 ou bicarbonato < 10mmol/L; e grave quando pH < 7,1 ou bicarbonato < 5mmol/L. Os níveis séricos de TSH (VR 0,35 – 4,94µlU/mL) e T4 livre (0,7 – 1,48ng/dl) e dos autoanticorpos tireoidianos anti-TPO (VR < 5,61UI/mL) e anti-TG (VR < 4,11UI/mL) foram obtidos por meio da técnica de quimioluminescência.
O diagnóstico de doença tireoidiana autoimune foi confirmado quando da presença de um ou mais autoanticorpos tireoidianos e o hipotireoidismo clínico foi diagnosticado quando, além da alteração citada, foram encontrados valores baixos do hormônio T4 livre; e/ou valores elevados de TSH; e/ou havia presença de bócio ao exame físico. Hipotireoidismo subclínico foi considerado quando havia valores normais de T4 e valores discretamente elevados de TSH.
Quanto aos autoanticorpos pancreáticos, os valores de anti-GAD foram obtidos pela técnica de enzimaimunoensaio (ELISA), sendo utilizados diferentes kits, com valores de referência para positividade quando > 5UI/mL ou > 10UI/mL; o ICA foi obtido por meio dos métodos de imunofluorescência indireta (VR < 1:4) e pelo ELISA (VR “não reagente”); para a mensuração dos níveis de IA-2A foram utilizadas as técnicas de radioimunoensaio (VR < 10UI/mL) e de ELISA (VR < 8UI/mL); e os valores de IAA foram obtidos pelos métodos de radioimunoensaio (VR < 0,4U/mL), radioimunoanálise (VR < 7,3%) e ELISA (VR < 8,6%).
A mensuração dos anticorpos anti-tTG IgA (VR < 20U/mL) e IgG (VR < 20U/mL) foi realizada pelo método ELISA; e a do antiendomísio (EMA) por imunofluorescência indireta (VR “negativo”). A dosagem sérica de IgA total foi feita pela técnica de turbidimetria, com valores de referência específicos para cada faixa etária (VR 0 a 3 meses: 1 – 34 mg/dL; > 3 meses a 1 ano: 8 – 91 mg/dL; > 1 ano a 12 anos: 21 – 282 mg/dL; > 12 anos: 65 – 421 mg/dL). Para aqueles pacientes que apresentaram deficiência de IgA total no momento do diagnóstico de DM1, a análise da autoimunidade para doença celíaca foi realizada por meio da detecção de anticorpos anti-transglutaminase tecidual da classe IgG.
A dosagem dos autoanticorpos pancreáticos foi realizada em laboratório conveniado e não pôde ser feita em alguns períodos do estudo, desta maneira, não foi avaliada em 100% dos pacientes. O EMA também não esteve disponível durante todo o período do estudo.
Os dados foram coletados entre julho de 2016 a agosto de 2017 em planilha eletrônica (Microsoft Excel®) e exportados para análise estatística no software Statistica v 10.0- Statsoft®. A estimativa da diferença de variáveis contínuas de distribuição normal foi realizada pelo teste paramétrico, teste t de Student, enquanto para variáveis de distribuição assimétrica, o teste não paramétrico, teste de Mann-Whitney e Anova de Friedman com teste post hoc de Mann-Whitney. A estimativa de diferença entre variáveis categóricas foi realizada pelos testes exato de Fisher e Qui-quadrado de Pearson. Para todos os testes, foi considerado um nível mínimo de significância de 5% e poder de teste mínimo de 90%.
A pesquisa foi aprovada pelo Comitê de Ética em Pesquisa em Seres Humanos da instituição sob CAEE. 32714314.8.0000.0096
RESULTADOS
Constituíram o grupo de estudo 92 crianças e adolescentes com diagnóstico novo de DM1, sendo 47 delas (51,1%) do sexo feminino. Características demográficas dos pacientes estudados estão dispostas na Tabela 1.

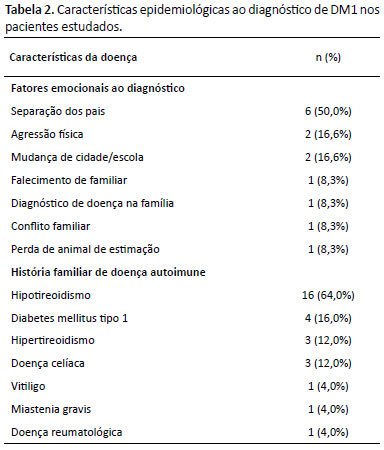
A mediana de idade ao diagnóstico foi de 8,5 anos, variando de 0,9 a 14,6 anos. Em 12 casos (13%), os pacientes ou seus familiares relataram a presença de fatores de estresse emocional à ocasião do diagnóstico de DM1, sendo o mais prevalente deles a separação conjugal dos pais (50%). Conforme ilustrado na Tabela 2, ao redor de um quarto dos indivíduos (27,2%) estudados apresentava história familiar positiva para doenças autoimunes, sendo o hipotireoidismo (64%) aquela encontrada com maior frequência.
No momento do diagnóstico de DM1, os pacientes apresentaram-se na vigência de CAD em 64,8% dos casos, sendo 23 (25%) deles casos leves, 16 (18,2%) casos moderados e 19 (21,5%) casos graves. À gasometria arterial, o pH médio foi de 7,28±0,14 e HCO3- mediano foi de 11,2, variando entre 1,5 e 24,9.
Com relação à positividade para autoanticorpos, a prevalência encontrada para aqueles associados às células beta-pancreáticas foi de 69,6% para o anti-GAD, 60,6% para IA-2A, 42,9% para o ICA e de 32,8% para IAA, sendo que em apenas 20% dos pacientes não foi detectada positividade para nenhum dos marcadores mencionados. Quanto à autoimunidade tireoidiana, foi detectada prevalência dos anticorpos anti-TPO e anti-TG de 13,1% e 22,9%, respectivamente, sendo que 10,7% do total de pacientes apresentava sorologia positiva para ambos.
Considerando os marcadores relacionados à doença celíaca, o anti-tTG IgA e o EMA foram aqueles encontrados com as menores taxas (12,5% e 6,0%). Os dados referentes à positividade dos auto anticorpos estão dispostos na Tabela 3.

Desta maneira, observou-se que entre os pacientes estudados 27,4% deles apresentaram, à ocasião da detecção do DM1, a coexistência de autoanticorpos para outras doenças autoimunes. A doença tireoidiana autoimune (DTAI) foi identificada como a comorbidade mais prevalente nas crianças diabéticas, estando presente em 21 (22,1%) pacientes, seguida pela doença celíaca com três (3,2%) e por vitiligo e alopecia, ambos presentes em um (1,05%) paciente.
Dentre os pacientes com acometimento tireoidiano, uma paciente apresentava hipotireoidismo clínico já previamente diagnosticado e outros três casos vieram a desenvolver a doença no seguimento clínico, com necessidade de reposição com levotiroxina, representando 19,0% dos pacientes com positividade para anti-TPO e/ou anti-TG. No acompanhamento da função tireoidiana, a primeira reavaliação foi realizada, em mediana, com 13,2 meses (7,1-17,1) e a segunda, com 25,8 meses (19,3-30,1).
Os níveis séricos dos hormônios TSH e T4 livre mantiveram-se, em mediana, sempre dentro dos valores de referência, não havendo diferença estatisticamente significativa entre os grupos com e sem positividade para quaisquer anticorpos (anti-TPO e/ou anti-TG). Também durante o seguimento, um paciente negativou seus níveis séricos de anti-TG e outros cinco pacientes apresentaram positividade para este anticorpo, em mediana com 12,4 meses, aumentando a prevalência da DTAI para 26,3%.
No que diz respeito à prevalência dos autoanticorpos de acordo com a idade dos pacientes, também não houve diferença estatisticamente significativa entre os grupos etários inferior a 5 anos, entre 5 e 9,9 anos e superior ou igual a 10 anos para quaisquer dos anticorpos (Teste exato de Fisher, p>0,05).
A positividade para o anti-GAD não revelou ser fator de predisposição à positivação ao longo do tempo dos pacientes ao anti-TPO (p=0,16) e ao anti-TG (p=0,24). Do mesmo modo, não foi possível observar a influência do sexo sobre a prevalência dos autoanticorpos contra a tireoide no momento do diagnóstico do DM1 (p=0,40). No entanto, após um ano de seguimento, observou-se tendência de associação positiva entre o sexo feminino e a positividade para tais anticorpos, sendo mais frequente a sua positivação quando em comparação aos pacientes masculinos (64% vs. 36%) (p=0,11), conforme demonstrado no Gráfico 1. Adicionalmente, a presença de um anticorpo tireoidiano indicou aumento da probabilidade de desenvolvimento de um segundo anticorpo (OR=27,9 p<0,001).
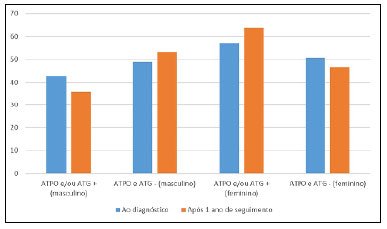 Gráfico 1. Positividade de auto anticorpos ao diagnóstico e após 1 ano de seguimento. anti-TPO = anticorpo antitireoperoxidase; anti-TG = anticorpo antitireoglobulina.
Gráfico 1. Positividade de auto anticorpos ao diagnóstico e após 1 ano de seguimento. anti-TPO = anticorpo antitireoperoxidase; anti-TG = anticorpo antitireoglobulina.No presente estudo descreveu-se o panorama de apresentação clínica dos pacientes pediátricos no momento do diagnóstico do DM1, com ênfase na análise da presença de marcadores de autoimunidade associada nestes indivíduos. A coexistência de outras DAI, além de representar um fator causador de morbidade, pode ainda exercer influências negativas no controle metabólico do DM1 ao produzir uma série de disfunções nos órgãos-alvo afetados8.
Como fator causal para essa forte associação entre as DAI, foi evidenciada a presença de uma origem genética comum entre elas (haplótipos de HLA), assim como de defeitos na regulação do sistema imunológico dos indivíduos acometidos, os quais acabam por apresentar risco consideravelmente elevado para o desenvolvimento de autoanticorpos contra diversos órgãos e tecidos, quando em comparação com a população em geral9.
Importantes na patogênese da destruição imunomediada das células beta produtoras de insulina, os autoanticorpos pancreáticos apresentam prevalências variáveis relatadas na literatura. Estudos brasileiros envolvendo crianças diabéticas demonstraram frequências amplamente distintas do anti-GAD, variando desde 5,9% até 80%4,10. O achado mais semelhante ao presente estudo foi a prevalência de 63,8% encontrada por Moreira et al. em uma população provinda da Região Sul do Brasil11. Considerando os outros autoanticorpos, foram relatadas frequências de aproximadamente 55% para o ICA, 35% para o IAA e de mais de 50% para o IA-2A, todas essas compatíveis com os achados deste estudo12-14.
Variações entre os resultados obtidos pelos diferentes pesquisadores podem ser explicadas pela utilização de variadas técnicas de detecção destes marcadores, com distintos valores de referência para mesmos anticorpos. Ainda assim, a literatura é convergente no que diz respeito ao achado de que o anti-GAD é o anticorpo encontrado, na grande maioria dos casos, com a maior prevalência dentre os marcadores de autoimunidade pancreática no momento do diagnóstico do DM16,9,12,15. Este fato aponta para a confirmação da teoria de que a descarboxilase do ácido glutâmico (GAD) seria o primeiro antígeno a agir como alvo da autoimunidade pancreática, ainda nos estágios iniciais e assintomáticos da doença16.
Com relação às outras doenças autoimunes, confirmou-se o achado de que a doença tireoidiana autoimune (DTAI), seguida da doença celíaca (DC), são aquelas encontradas com maior prevalência de associação ao DM15,6,14. No que se refere aos autoanticorpos contra a tireoide, ainda não está claro se eles são diretamente responsáveis pela patogênese da DTAI ou se surgem como resultado do processo de destruição da glândula mediado pela infiltração de células T. À parte disso, estudos internacionais demonstraram a prevalência destes marcadores oscilando entre 20 e 30%; em consonância com resultados observados em pacientes das regiões Nordeste e Sul do Brasil, respectivamente4,17. Neste trabalho, foram encontradas taxas próximas ao limite inferior de prevalência descrito na literatura.
A incapacidade de demonstração dos achados de associação positiva entre o sexo feminino e de idade mais avançada/maior tempo de doença com a presença de positividade para os anticorpos antitireoidianos pode ser explicada devido ao tamanho da amostra e ao curto período de seguimento dos pacientes após o diagnóstico de DM1, sendo este de apenas 12,4 meses, em mediana, para a análise da autoimunidade referente à tireoide15,17,18. Na evolução do acompanhamento, é possível que o número de pacientes com progressão para o hipotireoidismo clínico também se aproxime àquele relatado na literatura15,19.
Outra frequente associação encontrada na literatura entre as reações imunológicas anormais direcionadas concomitantemente ao pâncreas e à glândula tireoide diz respeito ao anti-GAD. Sua relação com os autoanticorpos tireoidianos pode ser explicada pelo fato de que o GABA, produto da reação enzimática desencadeada pelo seu antígeno (GAD), não está presente apenas no interior das ilhotas pancreáticas, mas também em diversos outros tecidos, como o cérebro, o estômago e a tireoide5,15.
Estudos transversais e longitudinais também foram capazes de demonstrar que pacientes com DM1 e DTAI apresentam níveis séricos mais elevados de anti-GAD em comparação com os pacientes sem DTAI e que a presença do anti-GAD em pacientes com DM1 aumenta em até duas vezes o risco para o desenvolvimento de DTAI quando em comparação com os indivíduos com sorologia negativa para este marcador12,18. Apesar de não atingir nível de significância estatística, nossos resultados demonstraram uma tendência à confirmação dessa associação positiva, por meio da análise de correlações entre a soroconversão do anti-GAD e do anti-TPO.
Quanto à doença celíaca, são relatadas taxas menos frequentes, variando mundialmente entre 1,6% e 12,3% dos casos, mas sendo, ainda assim, até 20 vezes mais frequente nos pacientes diabéticos comparando-se com o restante da população20. Dentre os indivíduos avaliados neste estudo, no momento da detecção do DM1 nenhum deles apresentou diagnóstico confirmado de DC, indo de encontro ao conceito de que a grande maioria dos casos (75-90%) é diagnosticada apenas pelos exames de rastreamento, anos após a evolução do diabetes21. Em crianças brasileiras, estudos relataram a prevalência de anti-transglutaminase tecidual entre 2,5% até 15,8%, tendo os casos confirmados de DC atingido a taxa de 3,1%; dados estes semelhantes aos resultados obtidos nesta pesquisa4,22.
Tempo de seguimento pós-diagnóstico de DM1, tamanho da amostra, diferenças nas técnicas laboratoriais e valores de referência dos exames e dificuldades processuais na realização dos exames de rastreamento podem ser citados entre as limitações do presente estudo, as quais poderiam explicar as divergências em relação aos dados encontrados na literatura.
CONCLUSÃO
Crianças e adolescentes com DM1 estão suscetíveis ao desenvolvimento de autoanticorpos, não apenas pancreáticos, mas também dirigidos a diversos outros tecidos e órgãos-alvo. A alta prevalência de associação do DM1 com outras doenças autoimunes, sobretudo a doença tireoidiana autoimune e a doença celíaca, indica a necessidade de realização rotineira de exames de rastreamento para estas comorbidades. A detecção precoce dessas doenças possibilita a aplicação de medidas para que repercussões negativas sobre o controle do DM1 e demais complicações sejam evitadas.
REFERÊNCIAS
1. Weber DR, Jospe N. Type 1 Diabetes Mellitus (Immune Mediated). In: Kliegman R, Saint Geme J, eds. Nelson Textbook of Pediatrics. 21st ed. Philadelphia: Elsevier; 2020. p. 3022-41.
2. Stanescu DE, Lord K, Lipman TH. The epidemiology of type 1 diabetes in children. Endocrinol Metab Clin North Am. 2012;41(4):679-94.
3. Sperling MA, Tamborlane WV, Battelino T, Weinzimer SA, Phillip M. Diabetes Mellitus. In: Sperling M, ed. Pediatric Endocrinology. Philadelphia: Saunders Elsevier; 2020.
4. Alves C, Santos L, Toralles MP. Association of type 1 diabetes mellitus and autoimmune disorders in Brazilian children and adolescents. Indian J Endocrinol Metab. 2016;20(3):381-6.
5. Krzewska A, Ben-Skowronek I. Effect of Associated Autoimmune Diseases on Type 1 Diabetes Mellitus Incidence and Metabolic Control in Children and Adolescents. Biomed Res Int. 2016;2016:6219730.
6. Kakleas K, Soldatou A, Karachaliou F, Karavanaki K. Associated autoimmune diseases in children and adolescents with type 1 diabetes mellitus (T1DM). Autoimmun Rev. 2015;14(9):781-97.
7. Wolfsdorf JI, Allgrove J, Craig ME, Edge J, Glaser N, Jain V, et al; International Society for Pediatric and Adolescent Diabetes. ISPAD Clinical Practice Consensus Guidelines 2014. Diabetic ketoacidosis and hyperglycemic hyperosmolar state. Pediatr Diabetes. 2014;15(Suppl. 20):154-79.
8. Shivaprasad C, Kolly A, Pulikkal A, Kumar KMP. High prevalence of organ specific autoantibodies in Indian type 1 diabetic patients. J Pediatr Endocrinol Metab. 2017;30(7):707-12.
9. Dayal D, Samprati M, Kaur N, Minz RW, Jayaraman D. Prevalence of beta-cell, thyroid and celiac autoimmunity in North Indian children with recent onset type 1 diabetes (T1D). J Clin Diagn Res. 2015;9(3):SM01-2.
10. Pardini VC, Mourao DM, Nascimento PD, Vivolo MA, Ferreira SR, Pardini H. Frequency of islet cell autoantibodies (IA-2 and GAD) in young Brazilian type 1 diabetes patients. Braz J Med Biol Res. 1999;32(10):1195-8.
11. Moreira MC, Lara GM, Linden R, Feksa LR, Tavares RG, Almeida SEM, et al. Frequency of the anti-glutamic acid decarboxylase immunological marker in patients with diabetes duration longer than three years in southern Brazil. Sao Paulo Med J. 2011;129(3):130-3.
12. Kawasaki E. Type 1 diabetes and autoimmunity. Clin Pediatr Endocrinol. 2014;23(4):99-105.
13. Lampasona V, Liberati D. Islet Autoantibodies. Curr Diab Rep. 2016;16(6):53.
14. Szypowska A, Błazik M, Groele L, Pańkowska E. The prevalence of autoimmune thyroid disease and celiac disease in children and adolescents with type 1 diabetes mellitus. Pediatr Endocrinol Diabetes Metab. 2008;14(4):221-4.
15. Karavanaki K, Kakleas K, Paschali E, Kefalas N, Konstantopoulos I, Petrou V, et al. Screening for associated autoimmunity in children and adolescents with Type 1 diabetes mellitus (T1DM). Horm Res. 2009;71(4):201-6.
16. Katsarou A, Gudbjörnsdottir S, Rawshani A, Dabelea D, Bonifacio E, Anderson BJ, et al. Type 1 diabetes mellitus. Nat Rev Dis Primers. 2017;3:17016.
17. Araujo J, Brandão LAC, Guimarães RL, Santos S, Falcão EA, Milanese M, et al. Prevalence of autoimmune thyroid disease and thyroid dysfunction in young Brazilian patients with type 1 diabetes. Pediatr Diabetes. 2008;9(4 Pt 1):272-6.
18. Kakleas K, Paschali E, Kefalas N, Fotinou A, Kanariou M, Karayianni C, et al. Factors for thyroid autoimmunity in children and adolescents with type 1 diabetes mellitus. Ups J Med Sci. 2009;114(4):214-20.
19. Piatkowska E, Szalecki M. Autoimmune thyroiditis in children and adolescents with type 1 diabetes. Pediatr Endocrinol Diabetes Metab. 2011;17(4):173-7.
20. Srivastava A, Chaturvedi S, Dabadghao P, Mathias A, Shukla U, Singh U, et al. Prevalence of celiac disease in Indian children with type 1 diabetes. Indian J Gastroenterol. 2016;35(5):372-8.
21. Camarca M, Mozzillo E, Nugnes R, Zito E, Falco M, Fattorusso V, et al. Celiac disease in type 1 diabetes mellitus. Ital J Pediatr. 2012;38:10.
22.Gonçalves CBCD, Silva IN, Tanure MG, Bahia M. Estudo da prevalência da doença celíaca em crianças e adolescentes com diabetes melito tipo 1: resultado de 10 anos de acompanhamento. Arq Bras Endocrinol Metab. 2013;57(5):375-80.
1. Universidade de São Paulo, Residente de Pediatria - São Paulo - São Paulo - Brasil
2. Universidade Federal do Paraná, Faculdade de Medicina - Curitiba - Paraná - Brasil
3. Universidade Federal do Paraná, Departamento de pediatria - Curitiba - Paraná - Brasil
Endereço para correspondência:
Felippe Gomes de Oliveira Ribas
Universidade de São Paulo
Av. Dr. Arnaldo, 455 - Cerqueira César
São Paulo - SP - Brasil. CEP: 01246903
E-mail: felippe.ribas1@gmail.com
Data de Submissão: 29/07/2021
Data de Aprovação: 20/08/2021
Recebido em: 29/07/2021
Aceito em: 20/08/2021


