O Nevo Melanocítico Congênito Gigante é uma doença rara1 representada por placas maiores que 20 cm, acastanhadas a negras, infiltradas, planas ou nodulares, cerebriformes, associadas ou não à hipertricose, que atinge preferencialmente tronco e membros superiores. Pequenas lesões pigmentadas, distribuídas pela pele, denominadas lesões-satélites, ocorrem em 78% dos casos2,3.
O diagnóstico é predominantemente clínico, porém alguns recursos auxiliam na investigação, como: histopatologia, imuno-histoquímica, tomografia computadorizada e ressonância magnética1.
As complicações mais temidas são a melanose neurocutânea (MNC) e o melanoma, as quais podem evoluir rapidamente e determinar um mau prognóstico para o paciente, nesses casos, as condutas e as intervenções devem ser precoces4. A abordagem terapêutica é multidisciplinar, exigindo seguimento permanente do paciente5.
RELATO DE CASOS
Os aspectos clínicos das lesões dos pacientes deste estudo foram descritos abaixo:
CASO 1: Sexo feminino, 1 ano, fototipo III, a apresentação clínica foi classificada com padrão de "calção de banho" (Figura 1A). A biópsia revelou padrão histopatológico compatível com nevo melanocítico.
CASO 2: Sexo masculino, 6 anos, fototipo IV, apresenta clinicamente o padrão de "bolero" (Figura 1B). Possui também desenvolvimento neuropsicomotor inadequado para idade com queixas de dificuldade de aprendizado e linguagem restrita, ainda em investigação diagnóstica. A histopatologia foi marcada pela proliferação de células névicas ovoides, formando ninhos com maturação para profundidade da lesão compatível com nevo melanocítico (Figura 2). Ressonância Magnética de Crânio e Coluna Vertebral sem alterações.
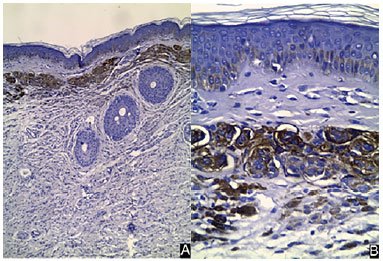 Figura 2. A histopatologia foi marcada pela proliferação de células névicas ovoides, formando ninhos com maturação para profundidade da lesão compatível com nevo melanocítico - Hematoxicilia eosina 10x; 2B Hematoxilina eosina 40x.
Figura 2. A histopatologia foi marcada pela proliferação de células névicas ovoides, formando ninhos com maturação para profundidade da lesão compatível com nevo melanocítico - Hematoxicilia eosina 10x; 2B Hematoxilina eosina 40x.CASO 4: Sexo masculino, 5 anos, fototipo IV, apresentação clínica classificada com padrão de "costas" (Figura 1D). O quadro se acompanhava de prurido intenso no nevo, sem outros sintomas. A histopatologia evidenciou proliferação melanocítica dermoepidérmica com atipias, porém, após análise imuno-histoquímica, os sinais de malignização foram excluídos. O resultado da ressonância magnética de crânio demonstrou focos de hipersinal, sem processo expansivo, compatível com melanose neurocutânea.
CASO 5: Sexo feminino, 4 anos, fototipo III, apresentação clínica foi classificada com padrão de "bolero" (Figura 1E). Após solicitação de exames complementares, a paciente não retornou para acompanhamento.
DISCUSSÃO
O Nevo Melanocítico Congênito Gigante afeta 1/20.000 a 1/50.0000 nascidos vivos, prevalecendo no sexo feminino1,2. Sua ocorrência se deve a mutações que geram rompimento da migração melanocítica da crista neural para a pele durante o desenvolvimento embrionário; quanto mais cedo esse evento ocorrer, maior será o tamanho do nevo6. Manifesta-se como mácula ou placa acastanhada e/ou negra, associadas ou não à hipertricose e rugosidades1. Lesões pigmentadas menores podem ocorrer na superfície cutânea, as quais, dependendo da concentração de melanina, podem ser marrom-claro, marrom-escuro ou negro4. O prurido se explica pelo estímulo das fibras sensitivas aferentes, a xerose e a hipo-hidrose à disfunção das estruturas anexiais1. No presente estudo, o sexo feminino foi prevalente e a maioria das crianças apresentavam prurido, xerose e mais de cinquenta lesões-satélites associadas.
É interessante sistematizar a distribuição das lesões, através da "Regra 6B"2, criando padrões: "bolero" (envolvendo a parte superior das costas, incluindo o pescoço), "costas" (nas costas, sem envolvimento das nádegas ou ombros), "calção de banho" (envolvendo a região genital e nádegas), "peito/barriga" (isolado no tórax ou abdômen, "extremidade do corpo", isolada à extremidade) e "corpo" (soma de dois padrões "bolero" e "calção de banho". A Figura 1 contém as imagens dos padrões da "Regra 6B" e sua correlação com os casos clínicos.
Essa classificação também inclui características adicionais2:
- Tamanho da lesão: Grande (L1: 20-30cm; L2: 30-40cm), Gigante (G1: mede 40-60cm; G2: maior que 60cm). Sendo o caso 1 e 4 classificados como G1 e os casos 2, 3 e 5 como G2.
- Grau de heterogeneidade da cor: C0 (nenhuma); C1 (moderado); C2 (marcante). Apenas o caso 1 foi classificado como C1, os demais foram classificados como C2.
- Hipertricose: H0 (nenhuma), H1 (notável), H2 (marcante). Apenas o caso 1 foi classificado como H1, os demais foram classificados como H2.
- Nodularidade: N0 (nenhuma); N1 (espalhadas); N2 (dérmica ou subcutânea extensa). Apenas o caso 5 foi classificado como N0, os demais foram classificados como N2.
- Número de lesões-satélites: S0 (nenhuma), S1 (menos de 20), S2 (entre 20-50), S3 (mais de 50). Apenas o caso 1 foi classificado como S1, os demais foram classificados como S3.
Apesar de o diagnóstico ser clínico, a biópsia com exame histopatológico deve ser recomendada. Os achados são: presença de melanócitos com morfologia variada na derme profunda, podendo atingir o tecido subcutâneo7.
Além de hiperqueratose e hiperplasia, alongamento das cristas epidérmicas associadas ao aumento do número de melanócitos e hiperpigmenação (alterações do tipo lentigo) e presença de melanócitos dispostos em ninhos na epiderme8 (Figura 2).
Associação com anormalidades como neurofibroma, vitiligo, lipoma e displasia do quadril pode ocorrer9, mais evidenciado no padrão de NMCG "corpo"10. O caso 3, com padrão "corpo", apresentou nódulos na região lombrossacra, cujo exame histopatológico evidenciou neurofibroma.
Múltiplas lesões congênitas satélites, ou aquelas de localização paravertebral ou axial, em dorso, cabeça ou pescoço estão associadas a um risco maior de desenvolvimento de melanoma, podendo ocorrer fora do nevo, em áreas ressecadas e outro órgãos11.
O caso 3 evoluiu com hemiplegia esquerda, seguida de óbito, por nódulo no cérebro que, após remoção do tumor, se obteve o diagnóstico de melanoma pela análise imuno-histoquímica.
Outra complicação vinculada ao NMCG é a melanose neurocutânea, caracterizada por proliferação melanocítica benigna ou maligna, em grande número, difusas ou nodulares nas leptomeninges do encéfalo ou na medula, que podem evoluir de forma assintomática ou com sintomatologia neurológica1. O caso 3, sem sintomas, teve sinais sugestivos e o caso 4 evidenciou focos de hipersinal no cérebro à RNM, sugestivo de NMC e segue assintomático.
Para o tratamento, considera-se localização, tamanho, profundidade, risco de malignização, envolvimento estético e psicológico12. Como opções: conduta expectante, crioterapia, dermobrasão, curetagem, laserterapia, ressecção seriada com enxertia, retalhos e expansão tecidual8. A expansão tecidual tem melhores resultados estéticos já que a área reconstruída tem uma correspondência de cor e espessura mais favorável em comparação com um enxerto de pele, sendo considerada o tratamento de escolha no NMCG localizado em cabeça e pescoço, tronco, coxa e ombros e a técnica preferida em nevo localizado em cabeça e pescoço pela importância estética13. É capaz de fornecer tecido doador local para grandes retalhos de pele, permitindo um melhor resultado da pele reconstruída e melhor posicionamento das cicatrizes com menor risco de retração e distorção anatômica13. Nesse registro, por serem crianças, com extensas áreas afetadas, adotou-se conduta expectante.
A conduta expectante consiste no acompanhamento clínico com periodicidade de 4 a 6 meses com o dermatologista, na realização de Ressonância Magnética de Crânio e Coluna anual, acompanhamento do desenvolvimento neuropsicomotor, e na biópsia com análise histopatológica de lesões suspeitas ou com alteração no aspecto clínico14. Além de medidas farmacológica para controle de sintomas, fotoproteção e hidratação da pele, alguns medicamentos podem ser associados para controle do prurido, entre eles o tremetinib (inibidor da MAP/ERK quinase), principalmente em portadores da mutação do gene BRAF15. O uso de inibidores de fosfatidilinositol-3-cinase (PI3K) e de inibidores Mitogen activated protein kinase (MAPK) podem ser tentados na presença de mutação NRAS15.
Durante o acompanhamento, alterações presentes podem exigir a realização de outros exames complementares, como a imuno-histoquímica, biópsia de linfonodo ou lesões expansivas e repetição da Ressonância Magnética com intervalo de tempo menor15.
Pelo exposto, conclui-se que o NMCG traz impacto psicossocial para os portadores e seus familiares, que requer acompanhamento multidisciplinar, cuja abordagem clínica e terapêutica permanece um desafio para a ciência.
REFERÊNCIAS
1. Viana ACL, Gontijo B, Bittencourt FV. Giant congenital melanocytic nevus. An Bras Dermatol. 2013;88(6):863-78.
2. da Silva VPM, Marghoob A, Pigem R, Carrera C, Aguilera P, Puig-Butillé JA. Patterns of distribution of giant congenital melanocytic nevi (GCMN): the 6B rule. J Am Acad Dermatol. 2017;76(4):689-94.
3. Endomba FT, Mbega CR, Tochie JN, Petnga SJN. Giant congenital melanocytic nevus in a Cameroonian child: a case report. J Med Case Rep. 2018;12(1):1-4.
4. Sawicka E, Szczygielski O, Żak K, Pęczkowski P, Michalak E, Bekiesińska-Figatowska M. Giant congenital melanocytic nevi: selected aspects of diagnostics and treatment. Med Sci Monit. 2015;21:123-32.
5. Han JS, Won CH, Chang SE, Lee MW, Choi J.H, Moon KC. Giant congenital melanocytic nevus with proliferative nodules mimicking a congenital malignant melanoma. An Dermatol. 2014;26(4):554-6.
6. Barysch MJ, Levesque MP, Cheng P, Karpova MB, Mihic-Probst D, Civenni G, et al. Coexpression of SOX10/CD271 (p75NTR) and β-Galactosidase in Large to Giant Congenital Melanocytic Nevi of Pediatric Patients. Dermatopathol (Basel). 2014;1(1):35-46.
7. Ciantelli GL, Steffen F de A, Lippi VG, de Morais LA, Jukemura D, das Eiras Tâmega I. Nevo melanocítico congênito gigante. Rev Fac Cienc Med Sorocaba. 2014;16(2):93-5.
8. Carneiro Junior LVDF, Aguiar LFDS, Pitanguy I. Tratamento cirúrgico do nevo melanocítico gigante. Rev Bras Cir Plást. 2011;26(2):198-204.
9. Shang Z, Dai T, Ren Y. Neurofibroma and lipoma in association with giant congenital melanocytic nevus coexisting in one nodule: a case report. Int J Clin Exp Med. 2015;8(7):11048.
10. Bhagwat PV, Tophakhane RS, Shashikumar BM, Noronha TM, Naidu V. Giant congenital melanocytic nevus (bathing trunk nevus) associated with lipoma and neurofibroma: Report of two cases. Indian J Dermatol Venereol Leprol. 2009;75(5):495-8.
11. Krengel S, Hauschild A, Schäfer T. Melanoma risk in congenital melanocytic naevi: a systematic review. Br J Dermatol. 2006;155(1):1-8.
12. Antonio CR, Antonio JR, de Oliveira Pozetti E, D'Avila SCGP, Cardeal ILS, Gerbi FC, et al. Nevus Pigmentado Piloso Gigante: Acompanhamento clínico e histopatológico de três anos após remoção com Laser Q-Switched Nd. YAG 1064mm. Surg Cosmet Dermatol. 2012;4(3):277-80.
13. Ruiz YG, Gutiérrez JCL. Multiple tissue expansion for giant congenital melanocytic nevus. An Plast Sur. 2017;79(6):37-40.
14. Grazziotin T. Nevos melanocíticos congênitos na infância. Boletim Científico de Pediatria. 2013;2(2):59-63.
15. Mir A, Agim NG, Kane AA, Josephs SC, Park JY, Ludwig K. Giant congenital melanocytic nevus treated with Trametinib. Pediatrics. 2019;143(3):e20182469.
1. Universidade do Estado do Pará (UEPA), Dermatologia - Belém - Pará - Brasil
2. Universidade do Estado do Pará (UEPA), Patologia - Belém - Pará - Brasil
Endereço para correspondência:
Bruna Cavaleiro de Macêdo Souza
Universidade do Estado do Pará
Rua Manoel de Abreu, s/nº, Mutirão
Abaetetuba, PA, Brasil
E-mail: brunacdms@gmail.com
Data de Submissão: 07/04/2021
Data de Aprovação: 18/05/2021
Recebido em: 07/04/2021
Aceito em: 18/05/2021



