A microangiopatia trombótica (MAT) resulta em oclusão dos vasos sanguíneos por trombos ricos em plaquetas, levando à trombocitopenia de consumo e anemia hemolítica. Essas alterações associadas à fragmentação das hemácias na microvasculatura, com formação de esquizócitos são essenciais para a suspeita. Podem estar presentes também aumento de lactato desidrogenase (LDH), teste de coombs negativo e coagulograma normal1.
Uma das causas mais importantes da MAT com consequente IRA em pediatria é a Síndrome Hemolítico-Urêmica (SHU), cuja etiologia clássica é a infecção por Escherichia coli OH157:H7 produtora de shiga toxina. A SHU pode também ser desencadeada pela infecção por Streptococcus pneumoniae e dessa forma denominada como Síndrome Hemolítico-Urêmica Atípica por Streptococcus pneumoniae (SHUa-Sp)1-3.
Em relação à doença pneumocócica, existe um amplo espectro de apresentações na infância e é a causa mais frequente de doença bacteriana invasiva nas crianças menores de dois anos após a introdução das vacinas contra Haemophilus influenzae tipo B e meningococo. A SHUa-Sp é uma complicação rara da infecção invasiva, porém apresenta alta taxa de morbimortalidade3,4.
Desde 2010, o calendário do Programa Nacional de Imunização (PNI) preconiza a vacinação infantil com a vacina pneumocócica conjugada 10-valente (VPC-10), com esquema de três doses: duas no primeiro ano de vida e uma dose de reforço aos 12 meses de idade. Em 2013, o PNI incorporou a vacina pneumocócica conjugada 13-valente (VPC-13), para pacientes específicos5-7.
RELATO DE CASO
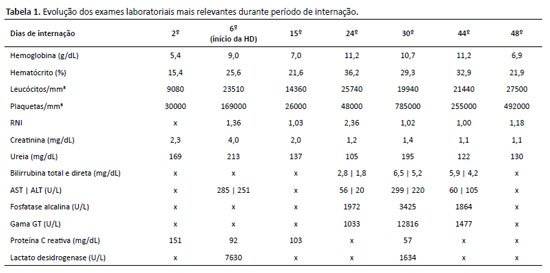
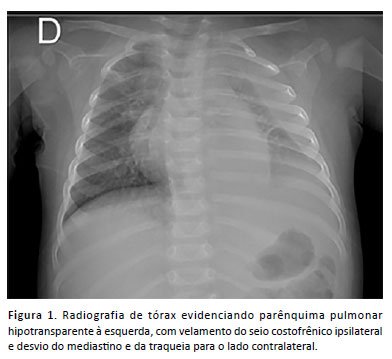
Lactente, sexo feminino, 9 meses, previamente hígida, vacinação adequada conforme PNI - VPC10 - admitida com sintomas gripais com evolução de três dias e piora progressiva. A propedêutica complementar evidenciou pneumonia complicada com derrame pleural (DP), leucocitose e aumento de provas inflamatórias (PCR e LDH) (figura 1) (tabela 1). Iniciada antibioticoterapia com Amoxicilina-Sulbactam conforme protocolo institucional, suporte ventilatório não invasivo e drenagem torácica.
Evoluiu com insuficiência respiratória, IRA KDIGo3, com oligúria e uremia; anemia, trombocitopenia e piora comparativa das provas inflamatórias. Modificada antibioticoterapia para Oxacilina+Ceftriaxona e encaminhada ao leito de terapia intensiva sob a hipótese de SHUa-Sp de foco pulmonar causado pelo Streptococcus pneumoniae subtipo 19A, identificado e tipado em cultura do líquido pleural.
Permaneceu em leito de terapia intensiva pediátrica por dois meses, em ventilação invasiva por 26 dias e terapia renal substitutiva. Demandou múltiplas transfusões de hemocomponentes, instabilidade hemodinâmica com necessidade de suporte vasoativo, além de icterícia colestática com alterações da função hepática e manifestações neurológicas, como crises convulsivas e hipertonia. Após estabilização, evoluiu para doença renal crônica (DRC) estágio 3b.
DISCUSSÃO
A avaliação inicial de um paciente com suspeita de MAT deve ser criteriosa para diferenciar síndromes primárias de outros distúrbios sistêmicos secundários. As causas primárias mais comuns são púrpura trombocitopênica idiopática e SHU e a importância da diferenciação justifica-se pela diferença no tratamento8.
A SHUa-Sp se dá pela ativação inadequada do sistema complemento através do estímulo gerado pela neuraminidase, enzima capaz de clivar o ácido n-acetil-neuramínico, constituinte das glicoproteínas das membranas celulares das células endoteliais, plaquetas, hemácias e células glomerulares. O antígeno-T também está presente nos hepatócitos, justificando a disfunção hepática transitória em alguns pacientes3,6,8-10.
Todos os sorotipos de pneumococo podem produzir neuraminidase, porém observa-se que os mais associados à SHUa-Sp são os 14, 6B, 9V, 19, 3, 8, 23F e 19A. Cada sorotipo é capaz de produzir quantidades diferentes dessa enzima com atividade metabólica diversa, sendo que o risco do desenvolvimento da SHUa-Sp é maior quanto maior carga bacteriana presente9,10.
Os pacientes com SHUa-Sp frequentemente apresentam pneumonia associada à empiema ou DP. A média de idade é entre 1-2 anos e a doença inicial é de apresentação grave. Geralmente a oligúria é prolongada, sendo necessária a terapia de substituição renal. Anemia e trombocitopenia graves demandam hemotransfusões frequentes. As complicações extrarrenais incluem colecistite, pancreatite, trombose, disfunção cardíaca e perda auditiva, como observado no caso11.
O foco primário da infecção pneumocócica deve ser tratado com antibióticos adequados. Ampicilina, Penicilina G ou Amoxicilina endovenosa são a primeira escolha para pacientes hospitalizados menores de cinco anos. Em pneumonias complicadas e com evolução grave apesar do uso de antibiótico com DP, empiema, pneumonia necrosante ou abscesso pulmonar, o tratamento deve ser individualizado. Em caso de DP, é necessário quantificar seu volume e qualificar seu estágio para a correta abordagem, seja ela expectante, drenagem de tórax, videotoracoscopia ou fibrinolíticos12.
O tratamento da SHU inclui suporte clínico para manutenção da estabilidade do paciente. Normalmente há necessidade de terapia renal substitutiva, manejo da sobrecarga hídrica e correções hidroeletrolíticas. Deve-se, também, corrigir anemias e trombocitopenias com hemocomponentes6,13.
A morbimortalidade relacionada à SHUa-Sp tem reduzido ao longo dos anos com os avanços nos cuidados suportivos e no diagnóstico precoce. A taxa de mortalidade é aproximadamente 11%-16% e é maior na fase aguda da doença, principalmente nos pacientes com a doença invasiva por meningite pneumocócica. Aproximadamente 25%-45% dos pacientes desenvolvem DRC e os fatores de risco mais importantes para essa sequela são a severidade da IRA e a necessidade de terapia de substituição renal por mais de 20 dias na fase aguda6.
Uma questão importante a ser considerada acerca das doenças pneumocócicas invasivas é a diminuição de sua prevalência em vários países durante a pandemia de COVID-19. As medidas de isolamento e higiene pessoal levaram à diminuição da transmissão e contágio de vírus e bactérias respiratórias em geral, incluindo o pneumococo. Essas medidas de contenção da disseminação do coronavírus ocasionaram a diminuição da colonização da nasofaringe pelos pneumococos, tendo como consequência a queda da imunidade inata. À medida que as medidas de distanciamento social e incentivo à higiene pessoal diminuíram, as crianças retornaram a ter contato com microrganismos de transmissão respiratória, porém sem a devida imunidade natural necessária para evitar doenças invasivas graves5.
Atualmente, no Brasil, duas vacinas pneumocócicas conjugadas estão disponíveis: VPC-10 e VPC-13. A primeira confere proteção contra os sorotipos bacterianos 1, 4, 5, 6B, 7F, 9V, 14, 18C, 19F e 23F e a segunda confere proteção contra os mesmos sorotipos, acrescidos ao 3, 6A e 19A. Entretanto, a VPC-13 é disponibilizada pelo SUS, porém restrita a imunossuprimidos. O imunobiológico amplamente distribuído como rotina na imunização infantil é a VPC105,6.
O PNI é um dos programas de imunização mais completos do mundo e assegura cobertura vacinal para diversos agravos, incluindo as doenças pneumocócicas. A VPC-10 está disponível no SUS, com redução estimada em 95% das doenças pneumocócicas causadas pelos sorotipos vacinais na população pediátrica menor de 5 anos, comparado ao período pré-vacinal. A ampla adesão à vacinação causou uma pressão seletiva e teve como resultado a mudança nos sorotipos identificados nas doenças invasivas, com aumento daqueles sem cobertura, principalmente os 3 e 19A5.
Correlacionando a literatura com o caso relatado, a paciente havia recebido a VPC-10 conforme preconizado pelo PNI, porém a doença invasiva pneumocócica foi causada em consequência da infecção pelo sorotipo 19A, presente apenas na VPC-13. A principal consequência dessa infecção foi a SHUa-Sp com suas complicações clássicas.
CONCLUSÃO
Apesar de não ser relatado na literatura o sorotipo de pneumococo mais frequentemente associado à SHUa-Sp, a paciente apresentava esquema vacinal completo pelo PNI, mas com evolução desfavorável causada pelo sorotipo 19A. Isso corrobora a importância da vigilância epidemiológica que permite conhecer o comportamento dos sorotipos circulantes na população brasileira e a incorporação contínua de vacinas mais abrangentes ao calendário nacional.
Adicionalmente, a Comissão Nacional de Incorporação de Tecnologias no Sistema Único de Saúde (CONITEC) publicou um relatório em novembro de 2022 referente à análise crítica das evidências científicas sobre a VPC13 para a prevenção da doença pneumocócica invasiva em pacientes de até 5 anos de idade, visando avaliar sua ampliação de uso no SUS. Foi possível observar que há evidências favoráveis ao efeito da VPC13 em comparação à VPC10, porém ainda é necessário comparar a efetividade das vacinas em relação ao resultado populacional da estratégia vacinal global para que haja a substituição completa da VPC10 pela VPC13.
REFERÊNCIAS
1. Thompson GL, Kavanagh D. Diagnosis and treatment of thrombotic microangiopathy. Int J Lab Hematol [Internet]. 2022; [cited 2023 Nov 16]; 44(S1):101–13. DOI: https://doi.org/10.1111/ijlh.13954. Available from: https://onlinelibrary.wiley.com/doi/10.1111/ijlh.13954.
2. Vilardouro AS, Cachão J, Rodrigues M, Durão F, Costa-Reis P, Sandes AR, et al. Hemolytic-uremic syndrome: 24 years’ experience of a pediatric nephrology unit. Braz J Nephrol [Internet]. 2022; [cited 2023 Nov 16]; 45(1):51–9. Available from : https://encr.pw/N9Lge.
3. Cestari AL de O, Vilela R, Kunisawa J, Lopes CE. Síndrome hemolítico-urêmica relacionada à infecção invasiva pelo Streptococcus pneumoniae. Rev Paul Pediatr [Internet]. 2008; [citado 2023 Nov 16]; 26(1):88–92. Disponível em: https://www.scielo.br/j/rpp/a/VgYkXxJmNVHzR55DTPvkpRt/.
4. Ferreira M, Oliveira H, Silva NC e., Januário L, Rodrigues F. Doença Invasiva Pneumocócica Pediátrica Antes da Vacinação Universal: 1995-2015. Acta Med Port [Internet]. 2017; [citado 2023 Nov 16]; 30(6):457–62. Disponível em: https://estudogeral.uc.pt/handle/10316/102202.
5. Vieira LMN. Pneumonia em crianças: novo desafio no ano de 2022. Rev Médica Minas Gerais [Internet]. 2022; [citado 2023 Nov 16]; 32(Supl 11):29–33. Disponível em: https://rmmg.org/artigo/detalhes/3962.
6. Agarwal HS, Latifi SQ. Streptococcus Pneumoniae-Associated Hemolytic Uremic Syndrome in the Era of Pneumococcal Vaccine. Pathogens [Internet]. 2021 Jun 9; [cited 2023 Dec 20]; 10(6):727. Available from: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8227211/.
7. Sociedade Brasileira de Imunizações. Calendário Nacional de Vacinação da Criança [Internet]. 2023 ago; [acesso em 2023 Dez 20]. Disponível em: https://sbim.org.br/calendarios-de-vacinacao.
8. George JN, Nester CM. Diagnostic approach to suspected TTP, HUS, or other thrombotic microangiopathy (TMA). Em: UpToDate [Internet]. 2023 jun; [cited 2023 Dec 20]. Available from: https://encr.pw/mR4gu.
9. Copelovitch L, Kaplan BS. Streptococcus pneumoniae-associated hemolytic uremic syndrome. Pediatr Nephrol [Internet]. 2008; [cited 2023 Nov 16]; 23(11):1951–6. DOI: https://doi.org/10.1007/s00467-007-0518-y. Available from: https://link.springer.com/article/10.1007/s00467-007-0518-y.
10. Battista M, Hoffmann B, Bachelot Y, Zimmermann L, Teuber L, Jost A, et al. The role of pneumococcal extracellular vesicles on the pathophysiology of the kidney disease hemolytic uremic syndrome. mSphere [Internet]. 2023; [cited 2023 Dec 20]; 8(4). DOI: https://doi.org/10.1128/msphere.00142-23. Available from: https://journals.asm.org/doi/10.1128/msphere.00142-23.
11. Niaudet P, Boyer OG. Overview of hemolytic uremic syndrome in children [Internet]. UpToDate. 2023 oct; [cited 2024 Jan 5]. Available from: https://acesse.dev/SmMgS.
12. Nascimento-Carvalho CM. Community-acquired pneumonia among children: the latest evidence for an updated management. J Pediatr (Rio J) [Internet]. 2020; [cited 2024 Jan 5]; 96(Suppl 1):29–38. Available from: https://pubmed.ncbi.nlm.nih.gov/31518547/.
13. Polito MG, Kirsztajn GM. Microangiopatias trombóticas: púrpura trombocitopênica trombótica e síndrome hemolítico-urêmica. J Bras Nefrol [Internet]. 2010; [Available from]; 32(3):303–15. Available from: https://www.scielo.br/j/jbn/a/zP9NxG6NfB5fRDjSL9SbQvM/?lang=pt.
1. Hospital Metropolitano Odilon Behrens, Residente de pediatria - Belo Horizonte - Minas Gerais - Brasil
2. Hospital Metropolitano Odilon Behrens, Coordenadora da residência de pediatria - Belo Horizonte - Minas Gerais - Brasil
3. Hospital Metropolitano Odilon Behrens, Emergencista pediátrica - Belo Horizonte - Minas Gerais - Brasil
4. Hospital Metropolitano Odilon Behrens, Intensivista pediátrica - Belo Horizonte - Minas Gerais - Brasil
Endereço para correspondência:
Julia Amaral Coimbra
Hospital Metropolitano Odilon Behrens
Rua Formiga, nº 50, São Cristóvão
Belo Horizonte, MG, Brasil. CEP: 31110-430.
E-mail: coimbra-julia@hotmail.com
Data de Submissão: 20/02/2024
Data de Aprovação: 25/06/2024
Recebido em: 20/02/2024
Aceito em: 25/06/2024