Os transtornos do espectro autista (TEA) são descritos pelo Manual Diagnóstico e Estatístico de Transtornos Mentais, Quinta Edição (DSM-5)1 como déficits persistentes de interação social e comunicação em vários contextos, acompanhados de padrões atípicos de comportamento, interesses ou atividades. Crianças com TEA podem apresentar sintomas como hiperatividade, automutilação, agressividade, inquietação, ansiedade, distúrbios do sono e sensibilidade sensorial, além de manifestações de hiper ou hipossensibilidade e reações a visões e sons específicos. Trata-se de um transtorno que pode causar sofrimento e desconforto para a criança e impactos negativos graves para a vida em família e na sociedade.2
Os sintomas podem variar em função da gravidade do transtorno, que inclui deficiências de comunicação social e comportamentos repetitivos e restritivos. Níveis de comprometimento mais elevados nessas áreas requerem maior suporte e indicam transtorno mais grave.1
O diagnóstico de TEA é costumeiramente feito durante o período pré-escolar, em crianças que apresentam atraso generalizado do desenvolvimento.3 A Academia Americana de Pediatria recomenda que todas as crianças sejam submetidas a testes de triagem específicos para autismo aos 18 e 24 meses, embora o diagnóstico possa ser feito mais precocemente em criança que satisfaçam os critérios diagnósticos.2 Quanto mais cedo o diagnóstico for feito, mais rápida será a introdução de intervenções terapêuticas, o que pode influenciar os resultados no desenvolvimento social e emocional e na qualidade de vida da criança.2
Até a presente data, o tratamento envolve uma abordagem multissensorial e multidisciplinar, com foco na independência funcional e na qualidade de vida da criança. Os tratamentos não farmacológicos visam minimizar os padrões atípicos de comportamento e aprimorar o desenvolvimento social e emocional. São trabalhadas as habilidades e a integração sensorial por meio de terapia ocupacional, assistência educacional, fonoaudiologia e terapia cognitivo-comportamental, além da promoção do reforço positivo com a família.4
Os tratamentos farmacológicos são individualizados e sintomáticos, incluindo antipsicóticos, antidepressivos, estabilizadores do humor, ansiolíticos, benzodiazepínicos e medicamentos para o sono. Os medicamentos se prestam a reduzir sintomas como irritabilidade, estereotipia e agitação psicomotora. Nenhum deles pode ser considerado uma cura para o transtorno, embora possam reduzir a maioria dos sintomas. Contudo, os efeitos colaterais podem ser consideráveis e levar os pais a não aderirem ao tratamento.5
Estudos recentes indicam que o canabidiol pode ser benéfico no manejo dos sintomas do TEA em crianças. A cannabis contém vários compostos quimicamente ativos, incluindo Δ9-tetrahidrocanabinol (Δ9-THC), canabidiol (CBD) e terpenoides, que interagem com o sistema endocanabinoide (SEC) no sistema nervoso central, afetando o apetite, a ansiedade, a função cognitiva e a memória.6
O SEC tem sido objeto de estudos por conta de sua capacidade de regular emoções e comportamentos sociais, por via dos receptores canabinoides (CB1 e CB2) e seus endocanabinoides, bem como das enzimas envolvidas em sua biossíntese e inativação. O SEC atua nos receptores canabinoides pré-sinápticos para reduzir a liberação de neurotransmissores como GABA, glutamato e acetilcolina. A disfunção nos componentes deste sistema pode contribuir para os déficits comportamentais e a neuroinflamação observados no autismo.7
O SEC desempenha um papel importante no desenvolvimento do sistema nervoso central (SNC). Seus receptores CB1 estão localizados no SNC, concentrados no cerebelo, hipocampo e gânglios da base, todas áreas de disfunção no autismo. Além disso, o autismo está associado à desregulação do sistema imunológico, que tem receptores CB2 nas células imunológicas e pode ter papel crítico na neuroinflamação relacionada ao TEA.7OBJETIVO
A presente revisão sistemática visa relatar os dados clínicos disponíveis sobre o uso de cannabis e canabinoides no tratamento dos sintomas comportamentais e comorbidades do TEA em crianças, além da potencial eficácia, tolerabilidade e segurança do CBD, considerando a evolução dos sintomas e a melhora clínica dos participantes dos estudos.
MÉTODOS
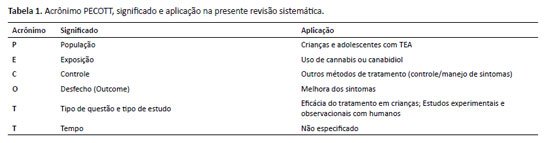
A questão da revisão definida pelo acrônimo PECOTT “O canabidiol é eficaz e seguro no tratamento de crianças com transtorno do espectro autista?” está representada na Tabela 1 a seguir.
Para responder à questão da revisão, usamos os descritores “Transtorno do Espectro Autista”, “tratamento”, “canabinoides” e “canabidiol” considerados conjuntamente com o Operador Booleano “AND” e os termos associados disponíveis no site Medical Subjects Headings (MeSH) identificados pelo operador booleano “OR”. Os termos foram utilizados para realizar buscas no PubMed, Cochrane Database of Systematic Reviews e Embase, sendo baixadas pesquisas disponíveis nessas bases.
Os critérios de inclusão foram estudos com crianças e adolescentes com Transtorno do Espectro Autista com idades entre 4 e 25 anos. Foram incluídos artigos publicados nos últimos 10 anos que fossem estudos observacionais ou experimentais com humanos. Excluímos artigos que não focassem no tratamento do TEA com canabidiol, assim como revisões.
Nosso objetivo é investigar se o canabidiol ou a cannabis são eficazes no tratamento e manejo dos sintomas do TEA em crianças e adolescentes. Como desfechos secundários, buscamos correlacionar os efeitos do canabidiol no prognóstico do transtorno e sua segurança.
Por meio de triagem e aplicação da questão PICO, selecionamos os artigos por título, resumo e leitura completa do artigo, respectivamente. Utilizamos o site Rayyan para a triagem, para organizar os motivos de inclusão e exclusão de artigos com mais facilidade, sem contabilizar erros de seleção. O processo foi duplo-cego e realizado por dois autores. As deficiências na segunda fase foram verificadas por um terceiro autor. Após a triagem, extraímos os dados que responderam ao nosso principal desfecho. Distribuímos os artigos selecionados pelo artigo completo para dois autores diferentes, que selecionaram dados de cada artigo e os salvaram em um arquivo do Google Docs. Um autor examinou cada artigo para garantir que informações sem importância fossem deixadas de fora.
RESULTADOS
Inicialmente, a busca, levou a 288 artigos, dos quais 56 eram duplicados, resultando em 232 artigos. Após a primeira triagem, 216 foram excluídos por não atenderem aos critérios de inclusão ou satisfazerem os critérios de exclusão. Dezesseis artigos foram incluídos com base no título para análise e leitura do texto completo, mas nove foram excluídos por não estarem disponíveis para leitura. No fim, foram incluídos sete artigos dos bancos de dados PubMed, Cochrane e Embase. A triagem está descrita na Figura 1 a seguir.
Seis dos artigos incluídos tinham Israel como país de origem. O sétimo estudo foi realizado no estado americano da Califórnia. A maioria usou o DSM-5 como critério diagnóstico para TEA. Contudo, os sintomas foram rastreados por diferentes instrumentos, como o Home Situations Questionnaire-ASD (HSQ-ASD); CGI-Improvement (CGI-I); Social Responsiveness Scale-2nd edition (SRS-2) e Autism Parenting Stress Index (APSI).
Dois ensaios clínicos randomizados analisaram placebo contra extrato de cannabis de planta inteira contendo CBD e THC em uma proporção de 20:1 e CBD puro e THC puro na mesma proporção e concentração. Um estudo observacional prospectivo analisou os resultados entre outros medicamentos e extrato de cannabis medicinal infundido em óleo de triglicerídeos de cadeia média (TCM) em proporção CBD:THC de 20:1. Um estudo retrospectivo usou apenas solução de óleo de canabinoide em concentração de 30% e proporção de 1:20 de CBD e THC, enquanto outro analisou azeite de oliva dissolvido com extratos de plantas inteiras com CBD e THC em proporção de 20:1. Um estudo observacional comparou THC (faixa de dosagem de 0,05–50 mg por dose) e CBD (faixa de dosagem de 7,5–200 mg por dose). Um estudo prospectivo analisou extrato de planta inteira infundido em óleo de TCM com proporção de CBD:THC de 20:1.
Os estudos selecionados estão representados na Tabela 2, onde constam autores, ano de publicação, tipo de estudo, tempo de seguimento, país do estudo e amostra, critérios de diagnóstico de TEA, pontuação de sintomas, intervenção e principais desfechos.
DISCUSSÃO
Alguns estudos reconhecem os transtornos do neurodesenvolvimento enquanto causa de morbidade em crianças, com efeitos sobre cognição, qualidade de vida, estresse parental e custos para a sociedade.15 Por esse motivo, a escolha do tratamento deve levar em conta o desempenho da criança nas áreas social, física, verbal e comportamental.
O tratamento padrão inclui antipsicóticos atípicos, inibidores seletivos da recaptação da serotonina, estimulantes e ansiolíticos. O objetivo não é a cura, mas sim a eliminação de sintomas. Na Europa, as opções terapêuticas aprovadas são aripiprazol e risperidona, medicamentos com eficácia e tolerabilidade subótimas em muitas crianças com TEA.6 Infelizmente, apenas 60% dos pacientes respondem bem aos tratamentos medicamentoso e comportamental convencionais.16
Aripiprazol e risperidona são medicamentos antipsicóticos atípicos que produzem efeitos colaterais semelhantes em crianças com TEA, tais como fadiga, aumento do apetite, sintomas gastrointestinais, hiperprolactinemia, ganho de peso e sedação. Esses medicamentos também podem causar efeitos colaterais graves, como dislipidemia, hiperglicemia, síndrome metabólica e sintomas extrapiramidais.17 A necessidade de abordagens terapêuticas inovadoras estimulou pesquisadores a explorar outras alternativas, como substâncias da Cannabis sativa, especialmente o canabidiol (CBD) e o Δ9-tetrahidrocanabinol (THC).
Um estudo randomizado foi conduzido em Israel com 150 crianças e adolescentes (5-21 anos) diagnosticados com transtorno do espectro autista (TEA), submetidos a tratamentos com placebo oral, extrato de cannabis de planta inteira contendo CBD e THC e CBD puro e THC puro. Os sintomas do TEA foram “graves” em 78,7% segundo o ADOS-2 e o nível adaptativo foi “baixo” (escore padrão ≤ 70) em 88% dos casos segundo a Escala de Comportamento Adaptativo de Vineland. O comportamento e os sintomas foram monitorados com os instrumentos HSQ-ASD, APSI, CGI-I e SRS-2. O estudo revelou que os escores totais do HSQ-ASD e do APSI não diferiram significativamente entre os participantes tratados com canabinoides e os que receberam placebo. No entanto, 49% dos 45 participantes que receberam canabinoides manifestaram resposta no CGI-I em comparação com 21% dos 47 que receberam placebo (p = 0,005). Além disso, houve melhora significativa na pontuação total do SRS-2 após tratamento com extrato de planta inteira em comparação com placebo (p = 0,009). Não houve eventos adversos graves relacionados ao tratamento segundo o Liverpool Adverse Events Profile (LAEP) modificado. No entanto, sonolência foi relatada como evento adverso leve significativamente relevante (p < 0,001).8
Os mesmos participantes do estudo anterior foram analisados para distúrbios do sono com o CSHQ. Entre os 146 participantes, 86% (n = 125) tinham distúrbio do sono (pontuação ≥ 41). Pontuações mais altas no CSHQ foram correlacionadas com idade mais jovem (p < 0,001) e pontuações totais mais altas no SRS (p = 0,036), indicando presença de traços autistas centrais mais graves. Apesar disso, as pontuações totais do CSHQ não diferiram significativamente entre os participantes que receberam canabinoides e os que receberam placebo. Da mesma forma, não houve diferença significativa entre os participantes que receberam o extrato da planta inteira versus canabinoides puros.9
Uma coorte prospectiva com 59 crianças e jovens adultos (idades de 5 a 25 anos) diagnosticados com TEA pelo DSM-5 e portadores de comorbidade grave, como problemas de sono, comportamentos de agressão/automutilação, ansiedade ou irritabilidade presentes há pelo menos seis meses, foi analisada com o objetivo principal de avaliar a segurança de um produto à base de óleo de cannabis rico em CBD por meio de exames de sangue. Nenhuma alteração significativa foi observada no hemograma completo, ureia ou creatinina, enzimas hepáticas (AST, ALT, ALP), hormônios da tireoide, anticorpos da tireoide, prolactina ou outros hormônios, antes e depois de três meses de tratamento. Os níveis de LDH estavam significativamente mais elevados antes em comparação a depois do tratamento (p = 0,003). Embora dentro da faixa normal, FT4 estava significativamente mais elevado após o tratamento (p = 0,03), enquanto TSH estava mais elevado antes do tratamento (p = 0,01). Os níveis de potássio (p = 0,04) foram alterados no grupo que recebeu medicamentos adicionais, como Aripiprazol e Metilfenidato, e no grupo tratado apenas cannabis medicinal. Comparando grupos que receberam CBD em baixa e alta dose, os níveis de proteína total foram significativamente mais elevados entre os que receberam altas doses (p = 0,01), embora a contagem de plaquetas fossem mais baixas entre eles (p = 0,0007). Nenhuma dessas alterações foi clinicamente significativa.10
Um estudo retrospectivo incluiu 53 indivíduos entre 3 e 25 anos de idade diagnosticados com TEA com base no DSM IV. Os pacientes receberam tratamento com canabidiol por um mês e foram avaliados para quatro sintomas de comorbidade do TEA: (a) sintomas de hiperatividade (b) problemas de sono, (c) automutilação e (d) ansiedade. Os efeitos adversos mais frequentes foram sonolência (n = 12) e diminuição do apetite (n = 6). Após a administração de canabidiol, os episódios de automutilação e ataques de raiva (n = 34) melhoraram em 67,6%, os sintomas de hiperatividade (n = 38) em 68,4%, os problemas de sono (n = 21) em 71,4% e a ansiedade (n = 17) em 47,1% dos casos. No entanto, não houve diferença estatisticamente significativa entre o tratamento convencional e o tratamento com canabidiol para automutilação (p = 0,063), sintomas de hiperatividade (p = 0,125), problemas de sono (p = 0,4) ou ansiedade (p = 0,232).11
Outro estudo conduzido em Israel incluiu 60 crianças entre 5 e 18 anos de idade diagnosticadas com TEA pelos critérios do DSM-5. Todas receberam tratamento com canabidiol e foram avaliadas usando os seguintes instrumentos: LAEP modificado, CGIC, HSQ-ASD e APSI. Alguns eventos adversos foram relatados pelos pais, como hipervigilância, inquietação, irritabilidade e perda de apetite. Em resumo, foi observada melhora considerável em problemas de comportamento (61%), ansiedade (39%) e problemas de comunicação (47%). Dos que foram tratados com medicamentos e cannabis concomitantemente, 20 (33%) receberam menos medicamentos ou dosagem menor, 12 (24%) pararam de tomar medicamentos e 4 (8%) necessitaram de mais medicamentos ou dose maior.12
Um estudo observacional realizado na Califórnia recrutou 24 crianças entre 6 e 12 anos de idade diagnosticadas com TEA. Elas foram tratadas com cannabis medicinal (n = 15) e comparadas com um grupo de crianças com desenvolvimento típico (n = 9) da mesma idade. O objetivo do estudo era identificar potenciais biomarcadores de resposta à cannabis e biomarcadores de resposta à cannabis que respondessem de forma diferente a diferentes tratamentos com cannabis medicinal. Foram identificados 65 potenciais biomarcadores de resposta à cannabis para TEA em 8 a 15 crianças com TEA. Além disso, 31 (48%) metabólitos foram detectados em todos os participantes e 21 (32%) exibiram mudança significativa (p < 0,05).13
Outro estudo prospectivo realizado em Israel analisou dados de 82 participantes entre 5 e 25 anos de idade tratados com cannabis rica em CBD. Todos satisfaziam os critérios do DSM-5 para TEA e relataram problemas comportamentais disruptivos durante os seis meses que antecederam o estudo. Houve melhora significativa nos escores de gravidade calibrados totais (CSS) do ADOS de 75 participantes avaliados antes e depois de seis meses de tratamento (p = 0,003), especialmente no afeto social (p = 0,001). Crianças com sintomas iniciais mais graves exibiram melhorias maiores (p = 0,002). Sessenta e um pacientes que completaram o questionário SRS-2 antes e depois do tratamento relataram melhora significativa nos principais sintomas do TEA (p = 0,043). Houve melhora significativa nas pontuações totais de Vineland em 76 crianças que concluíram o tratamento, principalmente em comunicação (p = 0,008), vida diária (p = 0,007) e socialização (p < 0,001).14CONCLUSÃO
Os estudos demonstram que os tratamentos com cannabis e canabinoides são métodos promissores e seguros para o alívio dos sintomas associados ao transtorno do espectro autista. Efeitos colaterais comuns incluem sonolência, hipervigilância, inquietação, irritabilidade e perda de apetite. Embora esses efeitos colaterais sejam geralmente considerados mínimos em comparação aos dos medicamentos tradicionalmente receitados para indivíduos com TEA com o mesmo fim (dislipidemia, hiperglicemia, síndrome metabólica e sintomas extrapiramidais), os efeitos de longo prazo do uso contínuo de cannabis e canabinoides em crianças ainda não foram elucidados. Apesar dos benefícios potenciais, é necessário ter cautela, principalmente em populações pediátricas. Mais estudos envolvendo coortes maiores são necessários para desenvolvermos orientações mais claras que fundamentem a tomada de decisões clínicas.
AGRADECIMENTOS
Os autores gostariam de expressar sua gratidão a todos os profissionais que contribuíram para a conclusão deste estudo.
CONFLITO DE INTERESSE
Os autores declaram não haver conflito de interesses.
REFERENCIAS
1. American Psychiatric Association. Diagnostic and Statistical Manual of Mental Disorders (DSM-5). 5th ed. Washington: American Psychiatric Association; 2013.
2. Hyman SL, Levy SE, Myers SM; COUNCIL ON CHILDREN WITH DISABILITIES, SECTION ON DEVELOPMENTAL AND BEHAVIORAL PEDIATRICS. Identification, Evaluation, and Management of Children With Autism Spectrum Disorder. Pediatrics. 2020;145(1):e20193447.
3. International Classification of Diseases, Eleventh Revision (ICD-11). Geneva: World Health Organization; 2021.
4. Zarafshan H, Salmanian M, Aghamohammadi S, Mohammadi MR, Mostafavi SA. Effectiveness of Non-Pharmacological Interventions on Stereotyped and Repetitive Behaviors of Pre-school Children With Autism: A Systematic Review. Basic Clin Neurosci. 2017;8(2):95-103.
5. Subramanyam AA, Mukherjee A, Dave M, Chavda K. Clinical Practice Guidelines for Autism Spectrum Disorders. Indian J Psychiatry. 2019;61(Suppl 2):254-69.
6. Dias-de Freitas F, Pimenta S, Soares S, Gonzaga D, Vaz-Matos I, Prior C. The role of cannabinoids in neurodevelopmental disorders of children and adolescents. Rev Neurol. 2022;75(7):189-97.
7. Babayeva M, Assefa H, Basu P, Loewy Z. Autism and associated disorders: cannabis as a potential therapy. Front Biosci (Elite Ed). 2022;14(1):1.
8. Aran A, Harel M, Cassuto H, Polyansky L, Schnapp A, Wattad N, et al. Cannabinoid treatment for autism: a proof-of-concept randomized trial. Mol Autism. 2021;12(1):6.
9. Schnapp A, Harel M, Cayam-Rand D, Cassuto H, Polyansky L, Aran A. A Placebo-Controlled Trial of Cannabinoid Treatment for Disruptive Behavior in Children and Adolescents with Autism Spectrum Disorder: Effects on Sleep Parameters as Measured by the CSHQ. Biomedicines. 2022;10(7):1685.
10. Stolar O, Hazan A, Vissoker RE, Kishk IA, Barchel D, Lezinger M, et al. Medical cannabis for the treatment of comorbid symptoms in children with autism spectrum disorder: An interim analysis of biochemical safety. Front Pharmacol. 2022;13:977484.
11. Barchel D, Stolar O, De-Haan T, Ziv-Baran T, Saban N, Fuchs DO, et al. Oral Cannabidiol Use in Children With Autism Spectrum Disorder to Treat Related Symptoms and Co-morbidities. Front Pharmacol. 2019;9:1521.
12. Aran A, Cassuto H, Lubotzky A, Wattad N, Hazan E. Brief Report: Cannabidiol-Rich Cannabis in Children with Autism Spectrum Disorder and Severe Behavioral Problems-A Retrospective Feasibility Study. J Autism Dev Disord. 2019;49(3):1284-8.
13. Siani-Rose M, Cox S, Goldstein B, Abrams D, Taylor M, Kurek I. Cannabis-Responsive Biomarkers: A Pharmacometabolomics-Based Application to Evaluate the Impact of Medical Cannabis Treatment on Children with Autism Spectrum Disorder. Cannabis Cannabinoid Res. 2023;8(1):126-37.
14. Hacohen M, Stolar OE, Berkovitch M, Elkana O, Kohn E, Hazan A, et al. Children and adolescents with ASD treated with CBD-rich cannabis exhibit significant improvements particularly in social symptoms: an open label study. Transl Psychiatry. 2022;12(1):375.
15. Hansen BH, Oerbeck B, Skirbekk B, Petrovski BÉ, Kristensen H. Neurodevelopmental disorders: prevalence and comorbidity in children referred to mental health services. Nord J Psychiatry. 2018;72(4):285-91.
16. Silva EAD Junior, Medeiros WMB, Torro N, Sousa JMM, Almeida IBCM, Costa FBD, et al. Cannabis and cannabinoid use in autism spectrum disorder: a systematic review. Trends Psychiatry Psychother. 2022;44:e20200149.
17. Aishworiya R, Valica T, Hagerman R, Restrepo B. An Update on Psychopharmacological Treatment of Autism Spectrum Disorder. Neurotherapeutics. 2022;19(1):248-62.
18. Page MJ, McKenzie JE, Bossuyt PM, Boutron I, Hoffmann TC, Mulrow CD, et al. The PRISMA 2020 statement: an updated guideline for reporting systematic reviews. BMJ. 2021;372:n71.
1. Faculdade de Minas (FAMINAS-BH), Acadêmica do curso de medicina - Belo Horizonte - Minas Gerais - Brasil
2. Faculdade de Minas (FAMINAS-BH), Médica pediatra e preceptora de Saúde da Criança e Adolescente - Belo Horizonte - Minas Gerais - Brasil
Endereço para correspondência:
Joice Rodrigues Rachid Amin
Faculdade de Minas (FAMINAS-BH). Av. Cristiano Machado, nº 12001, Vila Cloris
Belo Horizonte, MG, Brasil. CEP: 31744-007.
E-mail: joicerachid@hotmail.com
Data de Submissão: 06/02/2024
Data de Aprovação: 12/03/2025
Recebido em: 06/02/2024
Aceito em: 12/03/2025