A displasia broncopulmonar (DBP) foi inicialmente descrita por Northway et al.1 em 1967 considerando-se a necessidade de uso de oxigênio suplementar aos 28 dias de vida. Em 2001, o National Institute of Child Heath and Human Development (NICHD) trouxe uma nova definição, que considerava, além do uso de oxigênio suplementar por pelo menos 28 dias, a necessidade de verificar a dependência de oxigênio às 36 semanas de idade gestacional corrigida (IGC), no caso de prematuros nascidos com menos de 32 semanas de gestação e até os 56 dias de vida, ou momento da alta hospitalar, para os prematuros nascidos com mais de 32 semanas2.
A DBP é uma doença pulmonar crônica com características clínicas, radiológicas e histológicas próprias3. Além disso, é a complicação mais comum em prematuros, principalmente naqueles com muito baixo peso (<1500 gramas)4, afetando cerca de 30% dos prematuros menores de 32 semanas5 e 20-30% dos recém-nascidos muito baixo peso6.
Diferentes fatores que interagem, como prematuridade, ventilação mecânica, toxicidade do oxigênio, inflamação, infecção e genética podem resultar em interrupção do crescimento pulmonar. Porém, diferentes respostas de remodelamento pulmonar podem determinar as variações individuais de morbidade7. Esses pacientes apresentam aumento de mortalidade, e os que sobrevivem apresentam aumento da morbidade, piora na qualidade de vida e aumento de gastos com recursos5.
Sendo assim, o objetivo deste estudo é analisar os fatores de risco clínicos e epidemiológicos de prematuros com idade gestacional menor ou igual a 32 semanas e peso menor ou igual a 1500 gramas nascidos em um hospital da região metropolitana de Curitiba nos anos de 2018 até 2021 e verificar quais estão associados à DBP.
MÉTODO
Trata-se de um estudo transversal analítico e retrospectivo em que foram avaliados prontuários de pacientes nascidos em um hospital da região metropolitana de Curitiba nos anos de 2018 até 2021. No total, foram avaliados 6872 prontuários. Foram incluídos no estudo os que tinham idade gestacional menor ou igual a 32 semanas e peso menor ou igual a 1500 gramas. Foram excluídos os que foram a óbito no período neonatal. Desta forma, foram selecionados para esse estudo 54 pacientes.
Os dados coletados para análise descritiva da população foram: idade gestacional e materna, peso, pequeno para idade gestacional (PIG) de acordo com gráfico de Fenton (< p10)8, uso de corticosteroide antenatal, corioamnionite ou hipertensão arterial sistêmica (HAS) materna, gemelaridade, Apgar < 7 no quinto minuto de vida, parto vaginal, sexo masculino, intubação orotraqueal (IOT), massagem cardíaca ou adrenalina para reanimação na sala de parto de acordo com as normas da Sociedade Brasileira de Pediatria9.
Quanto à evolução neonatal, os dados foram relacionados à presença e à gravidade da DBP, sendo: DBP (necessidade de oxigênio suplementar aos 28 dias de vida), DBP leve (sem dependência de fração inspirada de oxigênio - FiO2 - complementar com 36 semanas de vida ou na alta, a depender do que ocorre primeiro), DBP moderada (FiO2 < 30% com 36 semanas de vida ou na alta) ou DBP grave (FiO2 > 30% ou pressão positiva com 36 semanas de vida ou na alta)2, além de outros dados: dias de internamento, alta com uso de oxigênio complementar, persistência do canal arterial (PCA) de acordo com laudo do ecocardiograma, tratamento cirúrgico ou medicamentoso caso houvesse PCA, enterocolite (de acordo com o Estadiamento de Bell Modificado)10, retinopatia da prematuridade, sepse (em caso de hemocultura positiva), hemorragia intraventricular (de acordo com laudo de ecografia transfontanelar), osteopenia e início de dieta enteral no primeiro dia de vida.
Além disso, foram pesquisadas também medidas quanto à necessidade de suporte respiratório: uso de CPAP na sala de parto, valor da FiO2 no 1º, 3º, 7º e 14º dia de vida, necessidade de ventilação mecânica invasiva (VMI) nesses mesmos dias, além da necessidade do uso de surfactante, cafeína e dexametasona do protocolo DART (Dexamethasone: A Randomized Trial)11 durante internamento.
Os dados obtidos foram processados em microcomputador, no banco de dados tipo Excel. Para a análise descritiva, nas variáveis quantitativas foram obtidas a média e o desvio padrão, enquanto na qualitativa foram as frequências absolutas e porcentagens. Foi considerado um nível de significância de 5%. Para a parte dos modelos, primeiramente foi utilizado o Teste Qui-quadrado ou teste exato de Fisher a fim de verificar as possíveis variáveis que deveriam manter- se no modelo. Foi realizado o modelo com todas as variáveis pesquisadas e, após isso, com as variáveis que apresentaram significância estatística. A área abaixo da curva ROC (AUC) foi calculada para os modelos finais. Para todas as análises, foi utilizado o software R na versão 4.1.2.
O presente estudo foi aprovado pelo Comitê de Ética em Pesquisa envolvendo seres humanos da instituição onde o estudo foi realizado (CAAE 5.111.870).
RESULTADOS
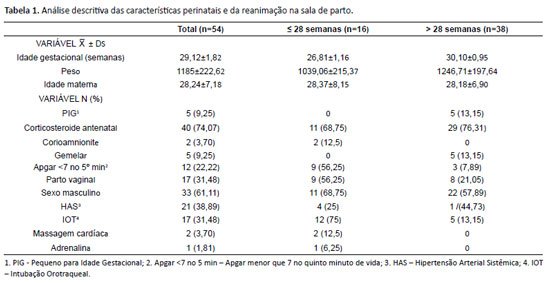
No período de 2018 a 2021, nasceram 54 pacientes com idade gestacional ≤ 32 semanas e com peso ≤ 1500 gramas e que não foram a óbito no período neonatal. Destes, 38 (70,37%) nasceram com mais de 28 semanas, sendo que a idade gestacional média foi de 29,12 semanas (±1,82) e o peso de 1185 gramas (±222,62). Em relação à idade materna para a amostra, a média foi de 28,24 anos (±7,18). A maior parte dos partos foi cesárea, sendo 31,48% via vaginal. Percebe-se que 61,11% da amostra era do sexo masculino e que 31,48% foi intubado já na sala de parto, conforme a Tabela 1.
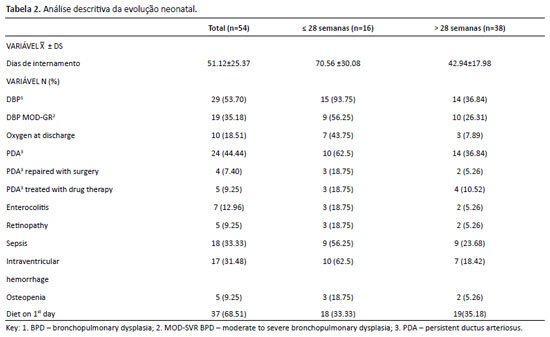
Já na Tabela 2, observa-se que o tempo médio de internamento foi de 51,12 dias (±25,37). O tempo dos pacientes ≤ de 28 semanas foi de 70,56 dias (±30,08), número consideravelmente maior do que o obtido nos ≥ de 28 semanas: 42,94 dias (±17,98), como esperado. Mais da metade dos pacientes incluídos no estudo (53,7%) desenvolveu DBP, mas em 35,18% ocorreu displasia broncopulmonar moderada-grave. Quando passa-se a dar destaque para a incidência de DBP nos pacientes com idade gestacional ≤ 28 semanas, nota-se que 93,75% desenvolveu DBP, enquanto nos pacientes com idade gestacional maior esse número foi de 36,85%. Um número significativo de paciente (18,51%) saiu do internamento hospitalar ainda necessitando do uso de oxigênio. Dos pacientes que tiveram PCA no laudo do ecocardiograma (44,44%), uma minoria necessitou de tratamento medicamentoso ou cirúrgico. Muitos pacientes tiveram complicações como sepse (33,33%), hemorragia intraventricular (31,48%), enterocolite (12,96%), retinopatia (9,25%), e osteopenia (9,25%), em ordem decrescente.
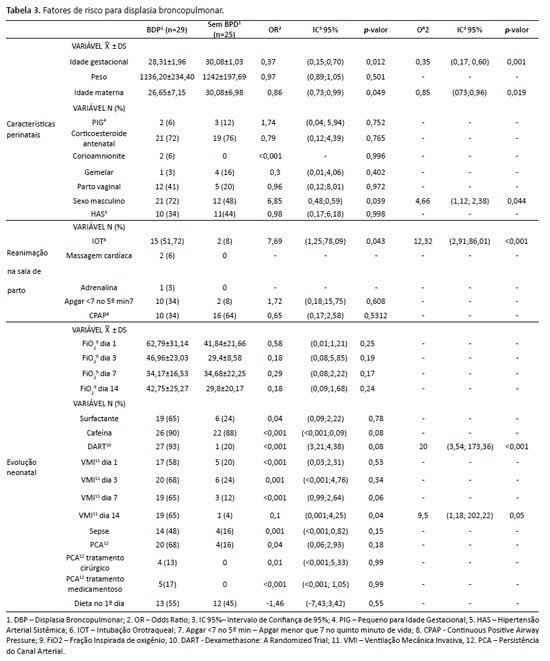
Quando comparamos paciente com e sem DBP em relação aos dados perinatais, observa- se na Tabela 3 que as variáveis de idade gestacional (OR: 0,35 e IC 95%: 0,17-0,60) (p=0,001), idade materna (OR: 0,85 e IC 95%: 073-0,96) (p=0,019) e sexo masculino (OR: 4,66 e IC 95%: 1,12-2,38) (p=0,044) tiveram significância estatística, ou seja, podem ser considerados fatores de risco para DBP. Ressaltando-se que ser do sexo masculino aumenta em 4,66 vezes a chance de ter DBP. Já se tratando dessa comparação em relação à assistência na sala de parto, a necessidade de IOT na sala de parto (OR: 12,32 e IC 95%: 2,91-86,01) (<0,001) mostrou-se significativa, aumentando em 12 vezes o risco. Em relação ao período de evolução neonatal, estar em VMI no 14º dia de vida (OR: 9,5 e IC 95%: 1,18-202,22) (p=0,05) e receber protocolo DART (OR: 20 e IC 95%: 3,54-173,36) (p<0,001) foram as variáveis consideradas estatisticamente significativas, aumentando em 9,5 e 20 vezes o risco, respectivamente.
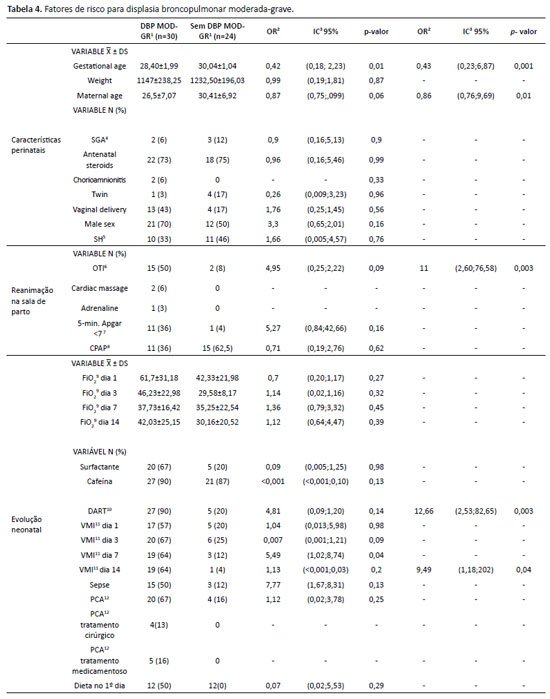
Já a Tabela 4 divide-se em grupos de pacientes que foram classificados como DBP moderada ou grave e pacientes sem DBP moderada ou grave (o que inclui aqueles que não tiveram DBP ou que a tiveram de forma leve). Desse modo, observa-se que idade gestacional (OR: 0,43 e IC 95%: 0,23-6,87) (p=0,001) e idade materna (OR: 0,86 e IC 95%: 0,76- 9,69) (p=0,01) são fatores de risco perinatais. Necessidade de IOT (OR:11 e IC 95%: 2,60-76,58) (p=0,003) também se mantém significativa quanto às variáveis de assistência na sala de parto, porém, nesse modelo, a IOT na sala de parto aumentou o risco em 11 vezes. Já as demais variáveis: VMI no 14º dia, protocolo DART e sexo masculino deixaram de se apresentar como fatores com significância estatística quando dividimos os grupos quanto a gravidade.
DISCUSSÃO
Observa-se que o aprimoramento da medicina tem sido responsável pelo aumento da sobrevida de prematuros de idades gestacionais cada vez menores. Portanto, discutir fatores que podem predizer doenças que alteram a morbimortalidade desse grupo passa a ser amplamente necessário também para avaliar os custos que isso pode gerar para o sistema de saúde.
No presente estudo, a incidência de DBP moderada-grave (35,18%) foi semelhante à demonstrada em países como Nova Zelândia/Austrália (34,3%) e Reino Unido (38,4%) no ano de 2015, conforme a rede de dados iNeo12. Porém, foi maior que a das unidades que compõem a Rede Brasileira de Pesquisas Neonatais, onde a incidência relatada foi de 19% para recém-nascidos prematuros com peso ao nascer < 1500 gramas13.
A incidência de DBP varia muito entre tantos artigos publicados, o que pode estar relacionado com fatores como o centro em que o recém-nascido é assistido, bem como as diferentes definições de DBP utilizadas em cada estudo. Porém, independentemente dessas variáveis, observa-se que sempre se sofre influência da idade gestacional ao nascer13, tendo em vista que o nascimento prematuro interrompe o desenvolvimento pulmonar programado.
Ao contrário do presente estudo, em que a idade materna e ser do sexo masculino aumentaram a chance de desenvolver DBP, outros não mostraram que essas variáveis têm significância estatística4,14,15. Já o peso ao nascer que se mostra como variável significativa na maioria dos estudos14,15, não se mostrou da mesma forma neste estudo. É provável que o resultado reflita a tendência de características da doença relacionadas ao menor peso ao nascer em um momento em que o tratamento pré-natal com corticosteroides está bem estabelecido4.
Em outra pesquisa14 a necessidade de IOT durante a reanimação em sala de parto já se mostrou um dado importante, tendo em vista que aumentou em 5,22 vezes (IC 95%: 2,25-12,1) (p<0,001) o risco de desenvolver DBP. Porém, nesse estudo, esse valor se mostra ainda maior: o risco aumentou em 12,32 vezes (OR: 12,32 e IC 95%: 2,91-86,01) (p<0,001).
É possível associar a maior duração de VMI e a ocorrência de DBP em outro estudo16 no qual é relatada a redução da incidência da doença com a diminuição do tempo de VMI. Já em outro artigo4, os prematuros com VMI ≥ 7 dias tiveram maior gravidade, mas se mostraram insignificantes na análise de regressão logística múltipla. Diferentemente dos anteriores, neste estudo, sugere-se que estar em VMI no 14º dia de vida é fator de risco isolado para desenvolver DBP, aumentando em 12,32 vezes o risco. Assim como o oxigênio, a ventilação mecânica parece ter grande importância na patogenia da DBP.
A lesão pulmonar induzida pela VMI é complexa, pois depende da interação entre a forma de ventilar e fatores intrínsecos do indivíduo. O barotrauma, volutrauma, atelectrauma e biotrauma podem ser determinantes, o que resulta em uma cascata inflamatória que interrompe as vias de sinalização envolvidas no desenvolvimento e na reparação pulmonar, contribuindo para o desenvolvimento da DBP17.
Os corticosteroides são potentes reguladores negativos de inflamação e são muito utilizados pós-natal para prevenir e tratar a DBP. Preocupações com os efeitos adversos dessa medicação, principalmente o comprometimento neurológico, no início dos anos 2000 levaram a recomendações contra seu uso18. Porém, evidência futura sugeriu que os benefícios poderiam superar os riscos quando o risco de DBP é alto (>50%)19. Atualmente, há muitas discussões a favor da prescrição de corticosteroides.
Outro estudo5, realizado na rede pública espanhola em 2021, também dividiu os pacientes com DBP moderada-grave e sem DBP moderada-grave. Mesmo tendo incluído um número maior de pacientes (202 pacientes) do que nesta pesquisa, a média de idade gestacional foi muito semelhante (29,5±2,1 anos), porém encontrou uma incidência menor de DBP (28,7%) e DBP moderada-grave (10,4%). Além disso, encontrou associação dessa doença com necessidade VMI no 5º dia de vida, sepse e FiO2 no 14º dia de vida. Quando se tratou de DBP moderada-grave, a associação foi com sepse e receber VMI no 3º e 5º dia de vida.
A sepse, apontada como fator de risco em tantos estudos5,14,15,20, não se mostra da mesma forma na atual pesquisa. Dados norte-americanos mostram que 36% dos recém-nascidos ≤ 28 semanas apresentam no mínimo um episódio de sepse, com até 50% de mortalidade. Na comparação com os que nascem a termo, a sepse em prematuros é muito mais frequente, sendo causa da mortalidade e alteração no desenvolvimento neurológico21, além de induzir inflamação e fibrose no pulmão de prematuros22.
Este estudo possui algumas limitações, principalmente relacionadas a ser retrospectivo e ter uma amostra relativamente pequena de pacientes (54 pacientes). A definição de DBP (dependência de oxigênio com 28 dias de vida) também pode ser um fator limitante, tendo visto que o Consenso do NICHD de 2021 fala em dependência de oxigênio durante 28 dias2.
Desta forma, através de dados clínicos coletados nesta pesquisa, conclui-se que mais da metade dos pacientes (53,7%) desenvolveu DBP, mas 35,18% teve displasia moderada-grave. A idade gestacional e materna, sexo masculino, necessidade de IOT na sala de parto, necessidade de VMI no 14º dia de vida e protocolo DART foram apontados como fatores de risco para a DBP, o que permite selecionar um grupo de recém-nascidos mais suscetíveis a essa doença. VMI no 14º dia, protocolo DART e sexo masculino deixam de ser fatores de risco quando selecionamos os pacientes com displasia moderada-grave. Este estudo pode servir de base para o desenvolvimento de outros modelos preditivos precoces e também para comparar a capacidade preditiva de novas ferramentas com as variáveis clínicas.
REFERÊNCIAS
1. Northway WH, Rosan RC, Porter DY. Pulmonary disease following respirator therapy of hyaline membrane disease. N Engl J Med. 1967;276(7):357-68.
2. Jobe AH, Bancalari E. NICHD/ NHLBI/ ORD Workshop Summary. Am J Respir Crit Care Med. 2001;163:1723-9.
3. Monte LF, Silva Filho LV, Miyoshi MH, Rozov T. Displasia broncopulmonar. J Pediatr. 2005;1:99- 110.
4. Jian M, He S, Liu Y, Liu X, Gui J, Zheng M, et al. Os fatores de alto risco de diferentes gravidades de displasia broncopulmonar (DBP) com base no instituto nacional de saúde infantil e desenvolvimento humano (NICHD): critérios de diagnóstico em 2018. J Bras Pneumol. 2021;47(5):e20210125.
5. Alonso AS, Díaz SP, Soto RS, Álvarez AA. Epidemiología y factores de riesgo asociados a displasia broncopulmonar en prematuros menores de 32 semanas de edad gestacional. Anal Pediatr. 2022;96(3):242-51.
6. Tapia JL, Agost D, Alegria A, Standen J, Escobar M, Grandi C, et al. Bronchopulmonary dysplasia: incidence, risk factors and resource utilization in a very low birth weight infant South- American population. J Pediatr. 2006;82(1):15-20.
7. Costa PFBM. Displasia Broncopulmonar. Pulmão RJ. 2013;22(3):37-42.
8. Fenton TR, Kim JH. A systematic review and meta-analysis to revise the Fenton growth chart for preterm infants. BMC Pediatr. 2013;13:59.
9. Guinsburg R, Almeida MFB. Reanimação do Prematuro <34 semanas em sala de parto: Diretrizes 2016 da Sociedade Brasileira de Pediatria [Internet]. São Paulo: Secretaria do Programa de Reanimação Neonatal da Sociedade Brasileira de Pediatria; [atualizado em 2016 Jan 26; citado em 2023 jan. 02]. Disponível em: https://www.sbp.com.br/fileadmin/user_upload/DiretrizesSBPReanimacaoPrematuroMenor34sema nas26jan2016.pdf
10. Walsh MC, Kliegman RM. Necrotizing enterocolitis: treatment based on staging criteria. Pediatr Clin North Am.1986;33(1):179-201.
11. Rademaker KJ, Groenendaal F, van Bel F, de Vries LS, Uiterwaal CS. The DART study of low-dose dexamethasone therapy. Pediatrics. 2007;120(3):689-90.
12. Lui K, Lee SK, Kusuda S, Adams M, Vento M, Reichman B, et al; International Network for Evaluation of Outcomes (iNeo) of neonates Investigators. Trends in Outcomes for Neonates Born Very Preterm and Very Low Birth Weight in 11 High-Income Countries. J Pediatr. 2019;215:32-40.e14.
13. Guinsburg R, de Almeida MF, de Castro JS, Silveira RC, Caldas JP, Fiori HH, et al. Death or survival with major morbidity in VLBW infants born at Brazilian neonatal research network centers. J Matern Fetal Neonatal Med. 2016;29(6):1005-9.
14. Tomé C. Incidência de displasia broncopulmonar em recém nascidos de muito baixo peso ao nascer e fatores associados [Dissertação de mestrado]. Santa Maria: Universidade Federal de Santa Maria, Centro de Ciências Sociais e Humanas, Programa de Pós-Graduação em Ciências da Saúde; 2018.
15. Freitas BAC, Peloso M, Silveira GL, Longo GZ. Prevalência e fatores associados à displasia broncopulmonar em hospital de referência para microrregião de Minas Gerais. Rev Bras Ter Intensiva. 2012;24(2):179-83.
16. Kwinta P, Grudzień A, Pawlik D, Olechowski W, Lauterbach R, Pietrzyk JJ. Prevalence and risk factors of bronchopulmonary dysplasia among extremely low birth weight newborns of regional birth cohort of south-east Poland. Przegl Lek. 2009;66(1-2):14-20.
17. Kalikkot Thekkeveedu R, Guaman MC, Shivanna B. Bronchopulmonary dysplasia: A review of pathogenesis and pathophysiology. Respir Med. 2017;132:170-7.
18. Committee on Fetus and Newborn. Postnatal corticosteroids to treat or prevent chronic lung disease in preterm infants. Pediatrics. 2002;109(2):330-8.
19. Doyle LW, Halliday HL, Ehrenkranz RA, Davis PG, Sinclair JC. An update on the impact of postnatal systemic corticosteroids on mortality and cerebral palsy in preterm infants: effect modification by risk of bronchopulmonary dysplasia. J Pediatr. 2014;165(6):1258-60.
20. Kim SH, Han YS, Chun J, Lee MH, Sung TJ. Risk factors that affect the degree of bronchopulmonary dysplasia: Comparison by severity in the same gestational age. PLoS One. 2020;15(7):e0235901.
21. Wynn JL. Defining neonatal sepsis. Curr Opin Pediatr. 2016;28(2):135-40.
22. Thomas W, Speer CP. Chorioamnionitis is essential in the evolution of bronchopulmonary dysplasia--the case in favour. Paediatr Respir Rev. 2014;15(1):49-52.
Hospital Angelina Caron, Serviço de Pediatria - Campina Grande do Sul - Paraná - Brasil
Endereço para correspondência:
Suelen dos Santos Henrique
Hospital Angelina Caron, Serviço de Pediatria
Campina Grande do Sul, Paraná, Brasil
E-mail: suelenhenrique@hotmail.com
Data de Submissão: 21/05/2024
Data de Aprovação: 17/09/2024
Recebido em: 21/05/2024
Aceito em: 17/09/2024