Em 2022, aproximadamente 10,6 milhões de pessoas no mundo contraíram TB, seguindo a tendência de alta desde o ano de 2020. Indivíduos de 0 a 14 anos representaram 8% dos novos casos1. No Brasil, foram notificados 81.604 novos casos em 2023, estando a faixa dos 0 aos 15 anos com tendência de aumento na incidência2. Após a infecção, o indivíduo pode eliminar o bacilo, evoluir para a forma latente, desenvolver TB pulmonar ou extrapulmonar e apresentar reações relacionadas à hipersensibilidade como a artrite de Poncet, eritema nodoso, tuberculides e a ceratoconjuntivite flictenular3-5. Descreve-se o caso de adolescente com história de febre e oligoartrite, cujo diagnóstico final foi AP.
RELATO DE CASO
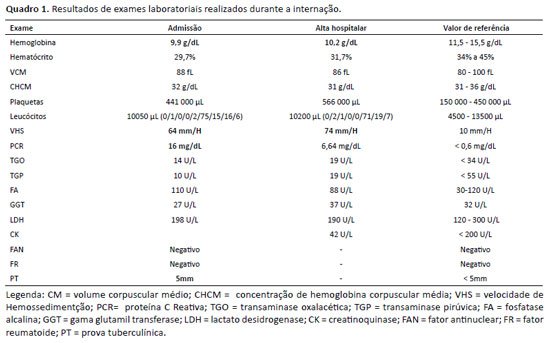
Adolescente, 14 anos, masculino. Dois meses antes da internação iniciou dor e rigidez matinal em quadril e joelho à direita que melhoravam com anti-inflamatórios não esteroidais (AINE). Passados cerca de 40 dias evoluiu com edema, piora da dor, impotência funcional e acometimento de articulações do tornozelo e AMTF do hálux à direita que melhoravam discretamente com uso de AINE, dor lombar que piorava com movimentação e melhorava ao repouso, além de febre vespertina (temperatura em média de 38,5 ºC) e sudorese. Nesse momento foi indicado internação. Referiu perda de peso não quantificada e contato recente com colega de jiu-jitsu em tratamento de TB pulmonar. Negava outros sintomas, comorbidades e infecções recentes. O histórico familiar era negativo. Cicatriz de BCG presente. Estava em regular estado geral, hipocorado, eupneico e anictérico. Peso igual a 60 kg (IMC = Z score >0 e <1). Apresentava claudicação, dor à mobilização do quadril à direita com diminuição do arco de movimento, edema, calor e dor em joelho, tornozelo e AMTF do hálux à direita. Restante do exame sem alterações. Evoluiu com febre e sudorese noturna diária, piora do quadro álgico necessitando uso de AINE de forma regular e perda de mais 2kg. Os resultados dos exames laboratoriais estão apresentados no quadro 1. Foram realizadas Biomicroscopia de fundo de olho, radiografia do tórax, ecocardiograma e ultrassonografia do abdome, todos normais. As sorologias para toxoplasmose, citomegalovírus, hepatites B e C, VDRL, Anti-HIV e hemocultura foram negativas, a ressonância magnética (RM) de quadril e joelho mostrou discreto derrame articular com as estruturas preservadas, sem erosão local e sem sinovite, e a de coluna lombossacra era normal. Não foi possível realizar dosagem de antígeno HLA-B27. Passados 60 dias do início do quadro, após a exclusão de outras causas de oligoartrite e com a história de contato para TB, PT positiva somado ao quadro de sudorese e febre, iniciou-se o esquema com rifampicina (R), isoniazida (I), pirazinamida (P) e etambutol (E) apesar de não identificado o sítio de TB doença. Permaneceu internado por mais 10 dias e após dois meses em acompanhamento ambulatorial evoluiu com melhora clínica, já não necessitando uso de AINE, que foi suspenso 2 semanas após início do esquema RIPE. Completou seis meses de tratamento e recebeu alta assintomático.
DISCUSSÃO
Trata-se de um paciente com oligoartrite crônica (envolvimento de quatro articulações com duração maior que 6 semanas) e sintomas sistêmicos (febre, sudorese noturna e perda ponderal), cujo diagnóstico diferencial inclui artrite idiopática juvenil subtipos relacionado à entesite (ARE) e sistêmico (AIJS), febre reumática (FRM), artrites reativas e, raramente, doenças linfoproliferativas, quando o paciente apresenta manifestações sugestivas, como linfonodomegalias, hepatoesplenomegalia e citopenias.
AIJS tem seu pico de incidência entre um e cinco anos, embora o diagnóstico seja possível em outras idades. As manifestações mais comuns são febre alta, artrite, exantema, linfadenopatia, hepatoesplenomegalia e serosite6. No caso relatado, não foi observado hepatoesplenomegalia, serosite ou exantema.
ARE requer a presença de artrite e entesite. Na falta de um deles, são necessários mais dois dos seguintes critérios: HLA B27 positivo; dor lombossacra inflamatória ou dor à digitopressão de sacroilíacas; uveíte anterior aguda; parente de primeiro grau com doença associada ao HLAB- 277. O paciente apresentava somente artrite e a dor lombar era mecânica. Mesmo na presença do antígeno HLA-B27 positivo, faltariam critérios para o diagnóstico de ARE.
Para FRM seria necessária a evidência de infeção pelo o Streptococcus ß-hemolítico do grupo A e presença de dois dos critérios maiores de Jones (cardite, poliartrite, coreia, eritema marginado, nódulo subcutâneo) ou um maior e dois menores (artralgia, febre, VHS >60 ou PCR >3, Intervalo PR prolongado)8. O paciente não apresentava histórico de infecções por Streptococcus ß-hemolítico do grupo A.
A artrite reativa cursa com mono/oligoartrite após alguma infecção sem que o agente possa ser isolado na articulação acometida. Os agentes mais comuns são bactérias que causam infecções gastrointestinais e ou geniturinárias. Em algumas situações pode ocorrer devido a germes atípicos9. A AP é um tipo de artrite reativa no contexto de infecção pelo Mtb10.
As arboviroses como dengue e chikungunya podem apresentar manifestações articulares. A chikungunya manifesta-se agudamente com febre alta, mialgia e artralgia simétrica intensas, principalmente nas extremidades como tornozelos, punhos e falanges. Apesar do padrão errático, costuma ser pior pela manhã, agravando-se com atividades físicas intensas11.
Quando surgiu a história de contato para TB, foi realizada radiografia de tórax (resultado normal) e a PT positiva. Após descartadas outras causas para artrite e como o paciente não apresentava manifestações clássicas de TB osteoarticular, como acometimento monoarticular e deformidade articular12, pensou-se em AP. Embora os exames de imagem não tenham identificado o sítio de acometimento da TB, optou-se por realizar tratamento para TB doença devido ao quadro de febre, sudorese noturna, perda ponderal, PT positiva e história epidemiológica. Rueda et al. (2013)13 demonstraram que em 3,5% dos casos de AP não foi encontrado o sítio de infecção pelo Mtb.
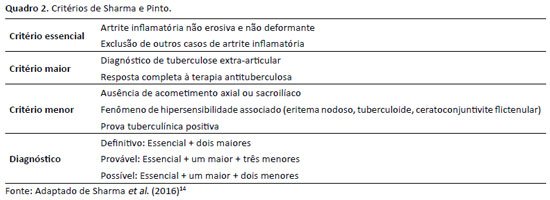
A AP é uma artrite reativa ao Mtb de acometimento oligo ou poliarticular, em que não há evidência de acometimento micobacteriano local e não se pode encontrar outra causa9. Acredita-se que ocorra devido à resposta imunomediada por células Th1, onde epítopos dos proteoglicanos da cartilagem humana são reconhecidos como proteínas de choque térmico do Mtb. Linfócitos Th1 e anticorpos alcançam a articulação, gerando a reação inflamatória13. Nesses casos, é esperado acometimento poliarticular e ausência de erosão local. Como a AP é uma doença rara e sem marcadores sorológicos específicos, Sharma et al. (2016)14 propuseram um critério diagnóstico para AP apresentado no quadro 2.
O primeiro sintoma apresentado foi a dor articular. Sharma et al. (2016)14 observaram que dor articular foi precedida pelo diagnóstico de AP em 87% dos casos. Este paciente apresentava oligoartrite (quadril, joelho, tornozelo e AMTF do hálux direito) não erosiva e não deformante. Em sua revisão de literatura com 198 casos de AP, Rueda et al. (2013)13 encontraram prevalência de oligoartrite em 40%, sendo tornozelo a articulação mais acometida, seguida de joelho, punhos e cotovelo. Shobha e Desai (2019)10 encontraram resultados semelhantes, assim como Sharma et al. (2016)14. A AP foi um diagnóstico de exclusão e presuntivo. O paciente apresentou dois critérios essenciais, um critério maior e dois menores segundo o critério diagnóstico de Sharma et al. (2016)14, configurando quadro diagnóstico possível de AP.
CONCLUSÃO
A TB é endêmica no Brasil, e na adolescência aumenta o risco de adoecimento15. A infecção pelo Mtb causa diversas manifestações clínicas. Na prática médica, revisar a história clínica pode trazer informações relevantes, como ocorreu no caso. A artrite de Poncet é rara e o diagnóstico é de exclusão, sendo necessário investigar outras causas de oligoartrite. Os critérios de Sharma et al. (2016)14 podem auxiliar na sua elucidação.
REFERÊNCIAS
1. World Health Organization (WHO). Global tuberculosis report 2023. Geneva: World Health Organization; 2023.
2. Ministério da Saúde (BR), Secretaria de Vigilância em Saúde e Ambiente, Departamento de HIV/Aids, Hepatites Virais e Infecções Sexualmente Transmissíveis. Boletim Epidemiológico - Tuberculose-2024. [Acesso em 2024 Mai 21]. Disponível em: https://www.gov.br/aids/pt-br/central-de-conteudo/boletins-epidemiologicos/2024/boletim-epidemiologico-tuberculose-2024/@@download/file
3. Dhattarwal N, Ramesh V. Tuberculids: A narrative review. Indian Dermatol Online J. 2023;14(3):320-9
4. Wiriyachai T, Boonsathorn S, Apiwattanakul N, Assawawiroonhakarn S. A rare case of primary sinonasal tuberculosis presented with phlyctenular keratoconjunctivitis in a pediatric patient: A case report and literature review. Medicine. 2021;100(7):1-4.
5. Drain PK, Bajema KL, Dowdy D, Dheda K, Naidoo K, Schumacher SG, et al. Incipient and Subclinical Tuberculosis: a Clinical Review of Early Stages and Progression of Infection. Clin Microbiol Rev. 2018 Jul 18;31(4):e00021-18.
6. Lee JJY, Schneider R. Systemic Juvenile Idiopathic Arthritis. Pediatr Clin North Am. 2018 Aug;65(4):691-709. DOI: https://doi.org/0.1016/j.pcl.2018.04.005.
7. Martini A, Ravelli A, Avcin T, Beresford MW, Burgos-Vargas R, Cuttica R, et al. Toward New Classification Criteria for Juvenile Idiopathic Arthritis: First Steps, Pediatric Rheumatology International Trials Organization International Consensus. J Rheumatol. 2019 Feb;46(2):190-7. DOI: https://doi.org/10.3899/jrheum.180168.
8. Pereira BAF, Belo AR, Silva NA. Febre reumática: atualização dos critérios de Jones à luz da revisão da American Heart Association - 2015. Rev Bras Reumatol. 2017;57(4):364-8.
9. Morris D, Inman RD. Reactive arthritis: developments and challenges in diagnosis and treatment. Curr Rheumatol Rep. 2012 Oct;14(5):390-4. DOI: https://doi.org/10.1007/s11926-012-0280-4.
10. Shobha V, Desai AM. Poncet's disease diagnostic criteria decodes conundrum: Poncet's vs pseudo Poncet's. Reumatismo. 2019 Apr 1;71(1):46-50. DOI: https://doi.org/10.4081/reumatismo.2019.1114.
11. Castro APCR, Lima RA, Nascimento JS. Chikungunya na a visão do clínico de dor. Rev Dor. 2016 Oct-Dec;17(4).
12. Agashe VM, Rodrigues C, Soman R, Shetty A, Deshpande RB, Ajbani K, et al. Diagnosis and Management of Osteoarticular Tuberculosis: A Drastic Change in Mind Set Needed-It is Not Enough to Simply Diagnose TB. Indian J Orthop. 2020 Jul 25;54(Suppl 1):60-70.
13. Rueda JC, Crepy MF, Mantilla RD. Clinical features of Poncet's disease. From the description of 198 cases found in the literature. Clin Rheumatol. 2013;32(7):929-35.
14. Sharma A, Pinto B, Dogra S, Sharma K, Goyal P, Sagar V, et al. A case series and review of Poncet's disease, and the utility of current diagnostic criteria. Int J Rheum Dis. 2016;19(10):1010-7.
15. Marais BJ, Gie RP, Schaaf HS, Hesseling AC, Obihara CC, Starke JJ, et al. The natural history of childhood intra-thoracic tuberculosis: a critical review of literature from the pre-chemotherapy era. Int J Tuberc Lung Dis. 2004 Apr;8(4):392-402.
1. Universidade Federal Fluminense, Médico residente em pediatria - Hospital Universitário Antonio Pedro - Niterói - Rio de Janeiro - Brasil
2. Universidade Federal Fluminense, Graduado em medicina - Niterói - Rio de Janeiro - Brasil
3. Universidade Federal Fluminense, Reumatologia pediátrica, Hospital Universitário Antonio Pedro - Niterói - Rio de Janeiro - Brasil
4. Universidade Federal Fluminense, Departamento materno-infantil, Faculdade de Medicina - Niterói - Rio de Janeiro - Brasil
Endereço para correspondência:
Douglas Castanheira Coelho
Hospital universitário Antonio Pedro
Av. Marquês do Paraná, 303, Centro
Niterói, RJ, Brasil. CEP: 24033-900
E-mail: pediatradouglas@gmail.com
Data de Submissão: 13/06/2024
Data de Aprovação: 19/08/2024
Recebido em: 13/06/2024
Aceito em: 19/08/2024