INTRODUÇÃO
A prematuridade, definida como o nascimento antes de 37 semanas de gestação, é um problema de saúde grave e crescente em todo o mundo. Dados da Organização Mundial da Saúde indicam que a prevalência de partos prematuros em todo o mundo varia de 5% a 18%. De 2011 a 2019, o Brasil registrou aproximadamente 3 milhões de partos prematuros, correspondendo a uma prevalência de 11%, colocando o país entre os dez com as maiores taxas de partos prematuros do mundo¹.
Bebês prematuros e de baixo peso ao nascer (BPN, <2500g) são muito suscetíveis a todas as complicações do parto prematuro tanto no período neonatal imediato quanto durante a infância² e são particularmente propensos a patologias orais, que são agravadas por complicações neonatais como defeitos no desenvolvimento e crescimento da região orofacial, incluindo dentes primários e permanentes e defeitos do desenvolvimento do esmalte (DDE), como hipoplasia do esmalte, opacidade do esmalte e hipomineralização molar-incisivo. Essas questões são mais prevalentes em prematuros, especialmente aqueles com <32 semanas ou bebês de muito baixo peso ao nascer (MBPN; <1500g), com defeitos do esmalte ocorrendo até três vezes mais frequentemente em comparação com bebês a termo3. A prevalência de DDE na dentição primária foi relatada em taxas que variam entre 13% e 45%, e pode chegar a 46% a 96% em crianças nascidas prematuras4.
A formação do esmalte começa aos 4 meses de gestação e continua até 11 meses após o nascimento, tornando-o suscetível a condições pré-natais, neonatais e pós-natais5. DDE são caracterizadas por irregularidades na qualidade e quantidade do esmalte dentário, resultantes de distúrbios ou danos ao órgão do esmalte. A maneira como esses defeitos se apresentam e sua gravidade geralmente dependem do estágio de desenvolvimento em que a ruptura ocorre, bem como da gravidade e duração da perturbação 6 . Hipoplasia do esmalte refere-se a um defeito quantitativo caracterizado pela deficiência do esmalte, enquanto a hipomineralização do esmalte representa um defeito qualitativo que envolve descoloração difusa, demarcada ou branca, amarela ou marrom com gravidade crescente à medida que a cor escurece5.
Esses bebês perdem o período de maior acúmulo mineral, que ocorre durante o último trimestre da gestação, e apresentam maior risco de defeitos no esmalte. Quase 80% do cálcio e do fósforo fetais são acumulados durante o terceiro trimestre da gestação, e quantidades significativas de minerais são acumuladas no tecido dentário durante a vida intrauterina, o que explica a deficiência mineral frequente em bebês prematuros. Essas deficiências são exacerbadas pela rápida depleção devido às demandas metabólicas de condições como doença óssea metabólica, sepse, persistência do canal arterial e hemorragia peri-intraventricular, comuns em bebês prematuros7.
A etiologia da DDE ainda não está totalmente esclarecida. Fatores potencialmente associados incluem status socioeconômico, tabagismo, hipertensão, diabetes gestacional, uso de medicamentos antiepilépticos durante a gravidez, infecção gastrointestinal por ancilostomíase e consumo de álcool. Um estudo brasileiro publicado em 2023 identificou uma redução nos níveis séricos da quimiocina RANTES em gestantes entre 22 e 25 semanas de gestação como um fator explicativo da DDE na dentição decídua. Essa descoberta sugere que a resposta imune materna pode ser um fator significativo no desenvolvimento de DDE nos dentes decíduos, ressaltando a necessidade de melhor manejo da saúde materna durante a gravidez para mitigar defeitos de desenvolvimento do esmalte8.
Um estudo longitudinal recente de 36 meses envolvendo 287 crianças prematuras de baixo peso ao nascer e 290 controles a termo descobriu que crianças prematuras de baixo peso ao nascer tinham uma incidência 3 vezes maior de hipomineralização molar-incisiva (HMI) e hipomineralização do esmalte (EH) em comparação ao grupo controle. Notavelmente, entre os 37 bebês RNMBP incluídos, a incidência de EH e HMI foi significativamente maior (86,5% e 70,3%, respectivamente) do que em controles a termo (26,9% e 21,7%, respectivamente). Essas descobertas destacam a maior vulnerabilidade de crianças prematuras de baixo peso ao nascer e RNMBP a defeitos do esmalte, ressaltando a necessidade de intervenções preventivas e terapêuticas focadas9. Além disso, um estudo de Feuser et al. envolvendo 84 crianças de dois a cinco anos mostrou que crianças de baixo peso ao nascer tinham significativamente mais dentes com DED em comparação com crianças a termo/peso normal ao nascer, sem diferença significativa na prevalência de cárie dentária. A admissão na unidade de terapia intensiva neonatal foi significativamente associada à presença de DED, enfatizando a necessidade crítica de cuidados especializados nessa população de alto risco10.
As DDEs têm implicações clínicas significativas, estando associadas a problemas como preocupações estéticas, hipersensibilidade dentária e aumento do risco de desenvolvimento de cáries. O reconhecimento da hipomineralização e das hipoplasias é crucial, visto que indivíduos afetados por essas condições necessitam de medidas preventivas e intervenção precoce11. Este estudo teve como objetivo avaliar a prevalência de defeitos de esmalte na dentição decídua de crianças prematuras de MBPN com idade entre 12 e 60 meses.
MATERIAIS E MÉTODOS
Este estudo transversal avaliou recém-nascidos prematuros egressos de unidades de terapia intensiva neonatal (UTIN) e posteriormente acompanhados em um ambulatório em Caxias do Sul, entre maio de 2019 e dezembro de 2020. Foram elegíveis para o estudo crianças com idade entre 12 e 60 meses, peso ao nascer inferior a 1500 g e idade gestacional inferior a 34 semanas. Os critérios de exclusão incluíram síndromes genéticas, malformações congênitas complexas, intervenções odontológicas prévias, ausência de dentes, condições odontológicas hereditárias, como amelogênese e dentinogênese imperfeita, e fluorose dentária.
Resultado e Variáveis
O desfecho primário, defeitos de desenvolvimento do esmalte, foi avaliado utilizando o Índice de Defeitos de Desenvolvimento do Esmalte Modificado, proposto pela Federação Odontológica Internacional em 1992. Variáveis demográficas adicionais foram coletadas, incluindo idade gestacional, peso ao nascer, duração da ventilação mecânica, sepse neonatal e doença óssea metabólica. Informações maternas como idade, tabagismo, escolaridade e comorbidades pré-natais também foram registradas, juntamente com dados pós-alta, incluindo a idade da erupção do primeiro dente e práticas de higiene bucal.
Coleta de dados
O consentimento informado foi obtido dos cuidadores de todos os participantes. Um exame odontológico intraoral completo foi realizado em cada criança por um único observador treinado sob condições de iluminação artificial, utilizando uma espátula de madeira e equipamento de proteção individual apropriado. Placa bacteriana e resíduos alimentares foram removidos, conforme necessário, com gaze esterilizada. A avaliação da cavidade oral foi documentada com registros fotográficos para posterior análise da consistência diagnóstica. A concordância entre os diagnósticos foi confirmada por meio de um alto nível de concordância (kappa = 0,7 [0,59 a 0,80]) com dois dentistas pediátricos externos. Cada criança foi incluída no estudo apenas uma vez, mesmo que tenha tido mais de uma consulta.
Análise Estatística
O tamanho da amostra foi calculado com base na prevalência descrita de DED variando de 52% a 96% em crianças de muito baixo peso ao nascer. Para atingir um poder de estudo capaz de detectar uma estimativa de prevalência de 65% com um intervalo de confiança (IC) de 95% e uma margem de erro absoluto de 10%, o tamanho da amostra necessário foi determinado em 88 participantes. Análises descritivas foram realizadas para determinar a prevalência de DED e a distribuição de tipos específicos de defeitos. Dados categóricos foram expressos como frequências, enquanto dados ordinais e numéricos foram apresentados como medianas e intervalos interquartis. As associações entre variáveis qualitativas foram examinadas usando o teste qui-quadrado ou exato de Fisher, com significância estatística definida em 5% (p < 0,05). Comparações de médias foram feitas usando o teste t de Student, e comparações de medianas foram feitas usando o teste U de M'ann-Whitney; Regressão logística multivariada foi usada para desenvolver um modelo de predição, incorporando variáveis com p < 0,2 e usando eliminação reversa para seleção de variáveis. A calibração do modelo foi avaliada pelo teste de Hosmer-Lemeshow e pela estatística C. Razões de chances (OR) com IC de 95% foram calculadas para potenciais variáveis preditoras. A análise dos dados foi conduzida utilizando o software R, versão 3.5.2.
Considerações éticas
O protocolo do estudo foi aprovado pelo Comitê de Ética em Pesquisa da Universidade de Caxias do Sul (número do protocolo 08128019.0.0000.5341) e foi conduzido de acordo com os padrões éticos da Declaração de Helsinque de 1975, revisada em 2013.
Resultados
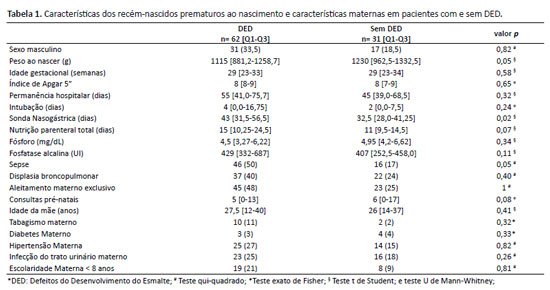
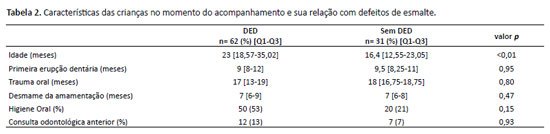
Durante o período do estudo, um total de 97 crianças atenderam aos critérios iniciais de elegibilidade. Foram excluídas uma criança com trissomia do cromossomo 21, uma que havia sido submetida a tratamento dentário restaurador e duas sem dentes erupcionados, resultando em uma população final de 93 participantes. As características clínicas e demográficas da população do estudo estão detalhadas nas Tabelas 1 e 2.
A DED foi observada em 62 crianças, representando uma prevalência de 67% (IC 95%: 57% a 76%). Diferenças significativas entre o grupo com DED e o grupo sem esse diagnóstico foram observadas na duração do uso da sonda gástrica (p = 0,02) e na idade no momento da consulta (p < 0,01).
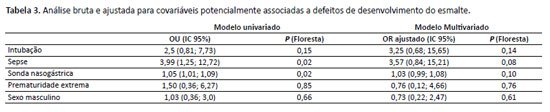
A análise de regressão logística univariada inicial identificou potenciais associações entre a ocorrência de DED e dois fatores: a presença de sepse tardia e a duração prolongada do uso da sonda. No entanto, essas associações não mantiveram sua significância estatística após o ajuste no modelo multivariado, que incluiu variáveis adicionais como sexo, idade gestacional, duração da intubação traqueal, duração do uso da sonda gástrica e sepse tardia (Tabela 3).
A hipoplasia emergiu como o defeito mais comum, afetando predominantemente os incisivos, seguidos por caninos e molares. Os incisivos também foram mais frequentemente impactados pela opacidade demarcada, seguidos por molares e caninos. Em contraste, a opacidade difusa foi mais prevalente em molares, depois caninos e incisivos. A análise revelou que os incisivos, seguidos por molares, foram mais comumente afetados quando a opacidade demarcada e a hipoplasia ocorreram simultaneamente. O pareamento de opacidade demarcada e difusa foi visto principalmente em molares, seguido por caninos, com o defeito mais raro sendo a opacidade difusa associada à hipoplasia, observada em caninos e depois molares. Ao examinar os arcos dentários, o arco superior mostrou uma maior incidência de DED, com incisivos, molares e caninos afetados em ordem decrescente. Por outro lado, os dentes menos afetados do arco inferior foram os caninos, seguidos por molares e incisivos. A distribuição de DED nessa população pode ser vista na Tabela 4.
DISCUSSÃO
Este estudo que examinou a prevalência de DED em uma coorte de 93 crianças nascidas prematuramente e com peso muito baixo ao nascer revelou três descobertas principais: uma prevalência de DED de 67%, uma tendência pronunciada de DED afetar os dentes incisivos superiores e hipoplasia do esmalte como a alteração mais frequente.
A taxa de prevalência observada de DED em 67% é consistente com a faixa de taxas de prevalência relatadas na literatura existente para bebês prematuros12-16. Ao contrário dos achados de outros estudos que identificaram uma relação inversa entre a idade gestacional e a prevalência de DED17, essa correlação não foi evidente em nossa investigação. Essa discrepância pode ser atribuída à concentração exclusiva de nosso estudo em bebês RNMBP, sem incluir grupos comparativos de bebês com pesos de nascimento mais altos. Além disso, a detecção de DED predominantemente em ambos os lados dos incisivos superiores contribui com novas perspectivas sobre as causas subjacentes desses defeitos. Isso implica que fatores sistêmicos, em vez de eventos traumáticos locais frequentemente associados à intubação orotraqueal, desempenham um papel significativo no desenvolvimento de DED3,18-19.
A proeminência da hipoplasia do esmalte é particularmente notável. O início precoce intrauterino da calcificação dos incisivos proporciona uma janela temporal vulnerável a distúrbios nutricionais e metabólicos20,21. O papel crítico da mineralização adequada, enfatizada por cálcio, fósforo, flúor, vitaminas A, C, D e proteínas, na prevenção da DED destaca o potencial das intervenções nutricionais pré-natais para mitigar o risco22-24.
Apesar de nossa rigorosa abordagem metodológica, certas limitações foram encontradas. A natureza retrospectiva de alguns dados coletados e a priorização da descrição da prevalência em detrimento da avaliação analítica em nosso cálculo amostral podem ter influenciado nossos achados. A alta prevalência de DED observada ressalta a necessidade urgente de estratégias preventivas direcionadas a essa população vulnerável. Além da contribuição epidemiológica de nosso estudo, o início paralelo de programas educacionais para pais e responsáveis e a facilitação do acesso a cuidados odontológicos pediátricos representam etapas fundamentais para mitigar os riscos à saúde bucal enfrentados por prematuros de muito baixo peso ao nascer.
Os achados deste estudo reforçam a significativa carga de DED em recém-nascidos prematuros de MBPN. A presença de DED provavelmente aumenta os riscos de desenvolvimento de cáries dentárias, aumento da sensibilidade dentinária e más oclusões. Se não tratadas, essas condições não apenas prejudicariam a saúde bucal, mas também o bem-estar geral e a qualidade de vida das crianças afetadas. A intervenção precoce, baseada em medidas clínicas e educacionais, é, portanto, fundamental para a promoção da saúde dessa população.
REFERÊNCIAS
1. Alberton M, Rosa VM, Iser BPM. Prevalência e tendência temporal da prematuridade no Brasil antes e durante a pandemia de covid-19: análise da série histórica 2011-2021. Epidemiol Serv Saúde [Internet]. 2023 Mar 31; [citado 2024 Aug 27]; 32(2):e2022603. Disponível em: https://www.scielo.br/j/ress/a/rR86nL5VqpNxFMKK47BRgsb/?format=pdf&lang=pt.
2. Merglova V, Dort J. Developmental enamel defects of primary incisors in preterm infants with very low and extremely low birthweight. A case-control study. Eur J Paediatr Dent [Internet]. 2020; [cited 2024 Aug 27]; 21(4):318-22. Available from: https://pubmed.ncbi.nlm.nih.gov/33337909/.
3. Bensi C, Costacurta M, Belli S, Paradiso D, Docimo R. Relationship between preterm birth and developmental defects of enamel: A systematic review and meta‐analysis. Int J Paediatr Dent [Internet]. 2020; [cited 2023 Sept 21]; 30(6):676-86. Available from: https://pubmed.ncbi.nlm.nih.gov/32243004/.
4. Halperson E, Shafir S, Fux-Noy A, Ram D, Eventov-Friedman S. Developmental defects of enamel in children born preterm. Front Pediatr [Internet]. 2022 Oct 13; [cited 2024 Aug 27]; 10:1019586. Available from: https://pubmed.ncbi.nlm.nih.gov/36313889/.
5. ark S, Jeong SJ, Han JH, Shin JE, Lee JH, Kang CM. Natal factors affecting developmental defects of enamel in preterm infants: a prospective cohort study. Sci Rep [Internet]. 2024 Jan 24; [cited 2024 Aug 27]; 14(1):2089. Available from: https://www.nature.com/articles/s41598-024-52525-2.
6. Salanitri S, Seow W. Developmental enamel defects in the primary dentition: aetiology and clinical management. Aust Dent J [Internet]. 2013 May; [cited 2024 Mar 28]; 58(2):133-40. Available from: https://onlinelibrary.wiley.com/doi/10.1111/adj.12039.
7. Merheb R, Arumugam C, Lee W, Collin M, Nguyen C, Groh-Wargo S, et al. Neonatal Serum Phosphorus Levels and Enamel Defects in Very Low Birth Weight Infants. JPEN J Parenter Enteral Nutr [Internet]. 2016 Jul 11; [cited 2024 Aug 27]; 40(6):835-41. Available from: https://pubmed.ncbi.nlm.nih.gov/25733338/.
8. Costa ER, Pinho JRO, Saraiva MCP, Ribeiro CCC, Batista RFL, Alves CMC, et al. RANTES and developmental defects of enamel in children: A Brazilian prenatal cohort (BRISA). PLoS One [Internet]. 2023 Jul 27; [cited 2024 Apr 4]; 18(7):e0284606-6. Available from: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10374131/
9. Mohamed RN, Basha S, Virupaxi SG, Eregowda NI, Parameshwarappa P. Hypomineralized Primary Teeth in Preterm Low Birth Weight Children and Its Association with Molar Incisor Hypomineralization-A 3-Year-Prospective Study. Children (Basel) [Internet]. 2021 Dec 2; [cited 2024 May 25]; 8(12):1111. Available from: https://pubmed.ncbi.nlm.nih.gov/34943307/.
10. Feuser E, Teixeira NM, Cruz PV, Bendo CB, Abreu LG, Paiva SM, et al. Developmental Enamel Defects and Dental Caries in the Primary Dentition of Preterm Children. J Dent Child (Chic) [Internet]. 2021 Jan 15; [cited 2024 May 26]; 88(1):40-5. Available from: https://pubmed.ncbi.nlm.nih.gov/33875051/.
11. Almeida Y, Carvalho TS, Bussaneli DG, Jeremias F. Congenital and acquired defects in enamel of primary teeth: prevalence, severity and risk factors in Brazilian children. Eur Arch Paediatr Dent [Internet]. 2021 Mar 12; [cited 2024 Aug 27]; 22(4):715-23. Available from: https://pubmed.ncbi.nlm.nih.gov/33710526/.
12. Arrow P, Piggott S, Jamieson L, Brennan D, Tonmukayakul U, Kularatna S, et al. Dental enamel defects and dental caries of primary teeth among Indigenous children in Western Australia. Aust Dent [Internet]. 2023; [cited 2024 Aug 27]; 68(1):35-41. Available from: https://pubmed.ncbi.nlm.nih.gov/36461644/.
13. Alshehhi A, Al Halabi M, Hussein I, Salami A, Hassan A, Kowash M. Enamel defects and caries prevalence in preterm children aged 5-10 years in Dubai. Libyan J Med [Internet]. 2020; [cited 2024 Aug 27]; 15(1):1705633.
14. Chaves AMB, Rosenblatt A, Oliveira OFB. Enamel defects and its relation to life course events in primary dentition of Brazilian children: a longitudinal study. Community Dent Health [Internet]. 2007 Mar 1; [cited 2024 Apr 22]; 24(1):31-6. Available from: https://pubmed.ncbi.nlm.nih.gov/17405468/.
15. Cruvinel VRN, Gravina DBL, Azevedo TDPL, Rezende CS, Bezerra ACB, Toledo AO de. Prevalence of enamel defects and associated risk factors in both dentitions in preterm and full term born children. J Appl Oral Sci [Internet]. 2012 Jun 1; [cited 2024 Apr 22]; 20(3):310-7. Available from: https://pubmed.ncbi.nlm.nih.gov/22858696/
16. Oliveira AFB, Chaves AMB, Rosenblatt A. The Influence of Enamel Defects on the Development of Early Childhood Caries in a Population with Low Socioeconomic Status: A Longitudinal Study. Caries Res [Internet]. 2006; [cited 2024 Apr 22]; 40(4):296-302. Available from: https://pubmed.ncbi.nlm.nih.gov/16741360/.
17. Takaoka LAMV, Goulart AL, Kopelman BI, Weiler RME. Enamel defects in the complete primary dentition of children born at term and preterm. Pediatric Dent [Internet]. 2011; [cited 2024 Apr 22]; 33(2):171-6. Available from: https://pubmed.ncbi.nlm.nih.gov/21703068/.
18. Nelson S, Albert JM, Geng C, Curtan S, Lang K, Miadich S, et al. Increased Enamel Hypoplasia and Very Low Birthweight Infants. J Dent Res [Internet]. 2013 Jul 15; [cited 2024 Apr 22]; 92(9):788-94. Available from: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3744269/.
19. Ruschel HC, Vargas-Ferreira F, Tovo MF, Kramer PF, Feldens CA. Developmental defects of enamel in primary teeth: highly prevalent, unevenly distributed in the oral cavity and not associated with birth weight. Eur Arch Paediatr Dent [Internet]. 2019 Mar 19; [cited 2024 Apr 22]; 20(3):241-8. Available from: https://pubmed.ncbi.nlm.nih.gov/30888582/.
20. Kim IH, Kang CM, Song JS, Lee JH. Dental complications associated with neonatal intubation in preterm infants. J Dent Anesth Pain Med [Internet]. 2019; [cited 2024 Apr 22]; 19(5):245-52. Available from: https://pubmed.ncbi.nlm.nih.gov/31723664/.
21. Diniz MB, Coldebella CR, Zuanon ACC, Cordeiro R de CL. Alterações orais em crianças prematuras e de baixo peso ao nascer: a importância da relação entre pediatras e odontopediatras. Rev Paul Pediatr [Internet]. 2011 Sep; [citado 2024 Abr 22]; 29(3):440-53. Disponível em: https://www.scielo.br/j/rpp/a/xnLNDW8pT5Wp5TgpqHm5Qzm/.
22. Franco KMD, Line SRP, Moura-Ribeiro MVL de. Prenatal and neonatal variables associated with enamel hypoplasia in deciduous teeth in low birth weight preterm infants. J Appl Oral Sci [Internet]. 2007 Dec 1; [cited 2024 Apr 22]; 15(6):518-23. Available from: https://pubmed.ncbi.nlm.nih.gov/19089191/.
23. Machado NF, Pereira JGM, Andrade DM de L, Gomes APM, Gomes AMM, Sarmento LC, et al. Defeitos de desenvolvimento do esmalte dentário na dentição decídua em crianças nascidas pré-termo e a termo. RBPS [Internet]. 2019 Jul 3; [citado 2024 Abr 22]; 21(1):72-9. Disponível em: https://periodicos.ufes.br/rbps/article/view/26470.
24. Mejias Velló, Martínez-Costa C, Catalá M, Fons J, Brines J, Guijarro-Martínez R. Prenatal and neonatal risk factors for the development of enamel defects in low birth weight children. Oral Dis [Internet]. 2010 Apr 1; [cited 2024 Apr 22]; 16(3):257-62. Available from: https://pubmed.ncbi.nlm.nih.gov/19849806/
1. Universidade de Caxias do Sul/Caxias do Sul/RS - Caxias do Sul - Rio Grande do Sul - Brasil
2. Programa de Pós-Graduação em Saúde da Criança e do Adolescente - Universidade Federal do Rio Grande do Sul - Porto Alegre - Rio Grande do Sul - Brasil
Endereço para correspondência:
Michelle Toscan
Programa de Pós-Graduação em Saúde da Criança e do Adolescente, Universidade Federal do Rio Grande do Sul,
Porto Alegre, Rio Grande do Sul, Brasil.
Rua Ramiro Barcelos, 2400, sala 220, em Porto Alegre,
Rio Grande do Sul, Brasil. E-mail: michelle.toscan@gmail.com
Data de Submissão: 25/06/2024
Data de Aprovação: 24/09/2024
Recebido em: 25/06/2024
Aceito em: 24/09/2024