A Leishmaniose Visceral (LV) — ou calazar — é uma patologia grave, sistêmica e potencialmente letal, com óbito em 90% dos casos não tratados1. Endêmica no Brasil, especialmente na região Nordeste, é considerada uma doença negligenciada, figurando entre as seis endemias prioritárias do mundo pela Organização Mundial de Saúde (OMS)1. As manifestações clínicas podem variar de formas oligossintomáticas a graves, e a diversidade de apresentações reflete a relevância da resposta imune4,6. A instalação do protozoário no fígado e no baço determina a hepatoesplenomegalia que, associada à pancitopenia decorrente de ocupação medular, e à febre pela etiologia infecciosa, torna essa condição um importante diagnóstico diferencial com doenças do sistema hematopoiético4,6. O espectro clínico pode incluir o acometimento pulmonar, considerado raro na literatura e de etiopatogenia ainda não claramente elucidada2. A relevância deste estudo está em suscitar o reconhecimento de formas clínicas atípicas de LV, aumentando o índice de suspeição diagnóstica em contextos incomuns e alertando para o possível subdiagnóstico de tal complicação.
RELATO DE CASO
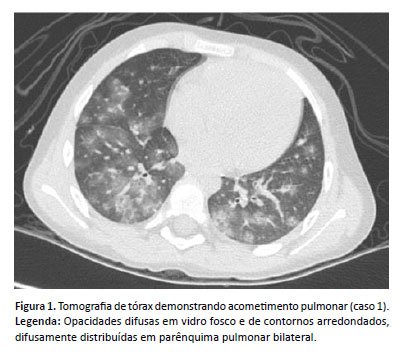
Caso 1: Paciente de 5 anos, sexo feminino, previamente hígida, iniciou quadro de febre recorrente de até 40 ºC, adinamia, hiporexia, palidez e perda ponderal (10kg em 20 dias). Após uma semana, evoluiu com hematúria e pancitopenia. Ao exame físico, apresentava hepatoesplenomegalia, e a ausculta pulmonar não evidenciava ruídos adventícios, assim como sinais de desconforto respiratório. Exames laboratoriais evidenciaram lesão hepática (AST 168 U/L [VR: <39U/L], ALT 72U/L [VR <42U/L], elevação de LDH (1.576U/L [VR: 140-271U/L]) e de ferritina (9.430 [VR: 9-148U/L]), hipoalbuminemia (2,8g/dL [VR: 3,5-4,8g/dL]) e inversão albumina/globulina (2,8mg/dL e 3,9mg/dL, respectivamente). Mielograma mostrou medula óssea hipocelular limítrofe para normocelular, com diseritropoese, disgranulocitopoese e presença de sinais de hemofagocitose. Imunofluorescência e teste-rápido para Leishmaniose foram positivos, sendo administrada Anfotericina B lipossomal 4mg/kg/dia por cinco dias, conforme protocolo do Ministério da Saúde5. Paciente manteve plaquetopenia grave (32.000 > 4.000 > 3.000 > 2.000 > 1.000/mm³ [VR: 140.000-440.000mm/³]), refratária à terapia transfusional, sendo associada corticoterapia. Após a suspensão da Anfotericina, paciente apresentou surgimento de crepitações à ausculta pulmonar, sem outros sinais ou sintomas associados. A radiografia de tórax evidenciou opacidade no terço inferior do pulmão direito. A tomografia de tórax com contraste mostrou opacidades difusas em vidro fosco e de contornos arredondados, difusamente distribuídas em parênquima pulmonar bilateral (figura 1). A paciente estava em uso de Ceftriaxona e Oxacilina há oito dias, mantidos até o décimo dia. Realizou painel viral respiratório para pesquisa de Influenza A e B e Coronavírus SARS-CoV-2, que resultou negativo. Aventada hipótese diagnóstica de pneumonite intersticial por Leishmaniose, apesar de não ser possível descartar componente hemorrágico. A paciente manteve-se assintomática do ponto de vista pulmonar, sem dispneia, hemoptise ou hipoxemia. Permaneceu com níveis plaquetários críticos (6.000/mm³), sendo administrada imunoglobulina humana endovenosa por dois dias, evoluindo com ascensão plaquetária (80.000/mm³). Recebeu alta para seguimento ambulatorial, com diagnóstico de Síndrome Hemofagocítica secundária à LV, plaquetopenia refratária com componente imune e pneumonite intersticial associada à leishmaniose. Retornou para reavaliação um mês após a alta, sendo repetida radiografia de tórax, sem alterações.
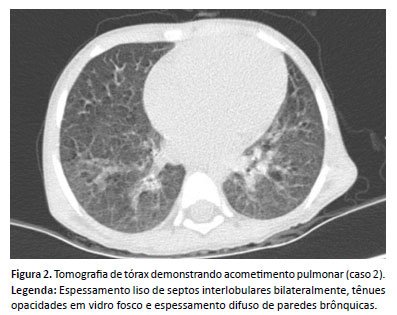
Caso 2: Paciente de três anos, sexo feminino, previamente hígida, iniciou, há três meses da admissão, quadro de febre (39 ºC) intermitente, sintomas gripais e dispneia, associado a aumento de volume abdominal, palidez e perda de peso (2kg). Foi encaminhada ao serviço de triagem de neoplasias devido à pancitopenia e hepatoesplenomegalia maciça, sendo hospitalizada. Realizou mielograma, que evidenciou presença de amastigotas, e teste-rápido rK39, que resultou positivo, sendo administrada Anfotericina B Lipossomal 3mg/kg/dia por sete dias, conforme protocolo do Ministério da Saúde5. Também fez uso de Ceftriaxona e Oxacilina por dez dias, devido à piúria em sumário de urina. Durante o tratamento, iniciou quadro de tosse produtiva, apresentando ausculta pulmonar com murmúrio rude e crepitações bolhosas difusas, tendo evoluído com redução da expansibilidade torácica e dispneia. Realizou tomografia de tórax com contraste, que evidenciou espessamento liso de septos interlobulares bilateralmente, tênues opacidades em vidro fosco e espessamento difuso de paredes brônquicas(figura 2). Na radiografia de tórax realizada dois dias após, evidenciou-se consolidação em ápice pulmonar e região peri-hilar direita. O painel viral respiratório foi realizado e resultou negativo. Apresentou melhora progressiva da sintomatologia respiratória, com tosse menos intensa e frequente por ocasião da alta hospitalar. Retornou para reavaliação após um mês e realizou nova radiografia de tórax, que não evidenciou alterações.
O envolvimento pulmonar na LV é raro e pouco descrito na literatura1-3, sendo aventada possibilidade de disseminação hematogênica da Leishmania — síndrome pseudo-Löffler —, reação de hipersensibilidade ocasionada por resposta imune exacerbada, infecção pulmonar secundária à imunodeficiência ou hemorragia pulmonar devido à plaquetopenia severa. As alterações parenquimatosas já descritas restringem-se à broncopneumonia e à pneumonite intersticial1, sendo esta a alteração histológica mais comum2,3. Nos casos descritos em literatura, o diagnóstico foi confirmado pelo isolamento do parasita em mielograma ou por provas séricas de imunofluorescência ou imunocromatografia positivas, e o envolvimento pulmonar foi considerado a partir de sintomatologia ou de alterações em exames de imagem1,3. Em apenas um caso há relato de confirmação histológica direta em tecido aspirado da lesão pulmonar2.
Quanto à sintomatologia, entre a literatura, a tosse é o achado mais comum, seguido por taquipneia e dor torácica1,3. A presença de sintomas respiratórios à admissão e seu surgimento durante o internamento indicam pior prognóstico em crianças, o que foi associado à possível infecção pulmonar concomitante1,3,5. As alterações radiológicas descritas tendem a convergir em achados relacionados à pneumonite intersticial1,3.
Em um estudo realizado no Nordeste brasileiro (2015-2018), envolvendo uma amostra de 42 pacientes, alterações tomográficas ocorreram em 59%, sendo 50% das imagens compatíveis com acometimento intersticial pulmonar (opacidades em vidro-fosco, opacidades reticulares e opacidades alveolares). A radiografia de tórax esteve alterada em apenas quatro pacientes1, o que pode indicar que ela nem sempre flagra as alterações. Neste estudo, houve associação estatística entre tosse seca e achados tomográficos [31,8% dos casos, p=0,047]. Os achados de exame físico não se associaram às alterações tomográficas e bioquímicas, e houve achados tomográficos que não haviam sido demonstrados por radiografia1.
Em outro estudo realizado no Nordeste brasileiro em 2021, com uma amostra de 22 pacientes pediátricos, houve sintomatologia pulmonar em 27,3% dos casos, sendo mais frequentes tosse e taquipneia. Alterações tomográficas foram encontradas em 50% dos pacientes, sendo mais frequentes opacidades em vidro fosco, opacidades reticulares, linfonodos residuais, opacidades alveolares e derrame pleural. Não foi descrita associação entre os sintomas respiratórios ou a faixa etária e as alterações tomográficas. Ademais, também foi demonstrado que a radiografia convencional de tórax não é capaz de detectar o comprometimento pulmonar da LV em sua totalidade3.
Um estudo iraniano de 2018 descreveu o caso de um paciente de 18 anos admitido com linfadenopatia submandibular, tosse seca e febre ocasional por cinco meses, associado à ausculta com estertores grossos e baqueteamento digital, sem outras alterações. A tomografia evidenciou consolidações broncopulmonares bilaterais maciças, com padrão nodular difuso. Realizou-se aspiração por agulha fina em nódulos pulmonares, com evidência de amastigotas na citologia. O diagnóstico foi corroborado por imunofluorescência positiva para anticorpos anti-leishmania em titulação 1:1024 e PCR para Leishmania positivo. A radiografia de tórax realizada três meses após o tratamento mostrou desaparecimento dos nódulos, entretanto surgiram múltiplas cavitações com paredes finas e infiltrado circundante, espessamento intersticial e pneumatoceles2.
Em nossa casuística, a tosse esteve presente apenas no caso 2, sendo inicialmente seca e tornando-se produtiva, concomitante ao surgimento de crepitações à ausculta pulmonar. Essa paciente evoluiu com taquipneia e dispneia leves, mas possuía, como fator confundidor, importante distensão abdominal, com redução da expansibilidade pulmonar. A despeito da clínica mais exuberante, apresentou alterações radiológicas menos significativas. Por outro lado, no caso 1, a alteração foi percebida apenas à ausculta pulmonar, sem achado de tosse, taquipneia, dispneia ou outros sintomas. Entretanto, houve alterações marcantes em exames de imagem, a despeito da pouca sintomatologia. Tal achado endossa a dissociação clínico-radiológica descrita em literatura1,3.
Conforme a literatura disponível, o comprometimento pulmonar pode ser precoce e estar implicado em desfechos clínicos desfavoráveis, tendo em vista que o processo inflamatório intersticial associado à fraca resposta macrofágica pode levar à broncopneumonia3. Outrossim, a pneumonia intersticial foi considerada potencialmente reversível, por ser a LV uma condição aguda e tratável1. Em nossa experiência, ambas as pacientes apresentaram normalização radiográfica cerca de um mês após o tratamento, corroborando a hipótese da reversibilidade do acometimento pulmonar na LV, em concordância com os estudos referenciados.
CONCLUSÃO
O envolvimento do sistema respiratório na LV é digno de atenção, pois pode ser subdiagnosticado mais comumente do que se conhece1. Trata-se de condição pouco descrita em literatura, e os relatos disponíveis resumem-se a achados clínicos e alterações radiológicas. Entretanto, já se sabe que a sintomatologia pode estar ausente mesmo diante de comprometimento pulmonar.
A confirmação definitiva de que alterações pulmonares se devam à LV per se encontra limitações técnicas, pois demanda a realização de procedimentos invasivos, indisponíveis na maioria dos cenários.
Os dois casos relatados endossam a dissociação clínico-radiológica relatada em literatura. Ainda, apresentam evolução pulmonar favorável e reversível, a despeito da ausência de terapia específica além do tratamento anti-leishmania, sugerindo que as alterações radiológicas relatadas tratem-se de manifestações da LV per se, embora a confirmação histológica não tenha sido passível de realização. Por fim, suscita-se que o acometimento pulmonar seja lembrado na abordagem do paciente com LV, visando a reduzir seu subdiagnóstico e a favorecer seu manejo adequado.
REFERÊNCIAS
1. Bispo AJ, Almeida ML, de Almeida RP, Bispo Neto J, Brito AVO, França CM. Pulmonary involvement in human visceral leishmaniasis: clinical and tomographic evaluation. PLoS One [Internet]. 2020 Jan; [cited 2024 Oct 1]; 15(1):e0228176. DOI: https://doi.org/10.1371/journal.pone.0228176. Available from: https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0228176.
2. Dehghani M, Monabati A, Sanei M, Davarpanah MA. Visceral leishmaniasis with massive pulmonary involvement: a case report. Int J Infect [Internet]. 2019 Feb; [cited 2024 Oct 1]; 6(1):e87993. DOI: https://doi.org/10.5812/iji.87993. Available from: https://brieflands.com/articles/iji-87993.
3. França CM, Bispo AJ, Azevedo LG, Silva LT, Almeida ML. Avaliação clínica e tomográfica em crianças portadoras de Leishmaniose Visceral Humana. Rev Eletronica Acervo Cient [Internet]. 2021 Maio; [citado 2024 Out 1]; 26:e7192. DOI: https://doi.org/10.25248/reac.e7192.2021. Disponível em: https://acervomais.com.br/index.php/cientifico/article/view/7192.
4. Bern C. Visceral leishmaniasis: Clinical manifestations and diagnosis. F Weller P, Bogorodskaya M, editors. UpToDate [Internet]. 2022 Feb; [cited 2024 Oct 1]; Available from: https://www.uptodate.com/contents/visceral-leishmaniasis-clinical-manifestations-and-diagnosis.
5. Ministério da Saúde (BR), Secretaria de Vigilância em Saúde, Departamento de Vigilância Epidemiológica. Leishmaniose visceral: recomendações clínicas para redução da letalidade. Brasília: Ministério da Saúde; 2011.
6. Costa DL, Costa CHN. Leishmaniose Visceral. In: Conceição-Silva F, Alves CR, comps. Leishmanioses do continente americano [online]. Rio de Janeiro: Editora FIOCRUZ; 2014:327-53. DOI: https://doi.org/10.7476/9788575415689.0020.
1. Hospital Infantil Albert Sabin, Pediatria - Fortaleza - Ceará - Brasil
2. Hospital Infantil Albert Sabin, Infectologia Pediátrica - Fortaleza - Ceará - Brasil
3. Universidade Federal do Ceará, Faculdade de Medicina - Sobral - Ceará - Brasil
4. Universidade Estadual do Ceará, Faculdade de Medicina - Fortaleza - Ceará - Brasil
Endereço para correspondência:
Raabe de Jesus Souza
Hospital Infantil Albert Sabin.
Rua Tertuliano Sales, 544 - Vila União, Fortaleza - CEP, 60410-794.
E-mail: jsouzaraabe@gmail.com
Data de Submissão: 01/10/2024
Data de Aprovação: 28/11/2024
Recebido em: 01/10/2024
Aceito em: 28/11/2024


