INTRODUÇÃO
A veia porta pré-duodenal (VPPD) é uma rara anomalia congênita que foi descrita pela primeira vez em 19211.
É causada pelo desenvolvimento embrionário anormal. A veia porta (VP) é formada pela união das veias mesentéricas, em torno do nível da segunda vértebra lombar, anterior para a veia cava inferior e posterior para o pâncreas2. Em seguida, segue superior e posterior à primeira parte do duodeno. Ao nível do fígado, divide-se em um ramo esquerdo e direito.
Durante vida embrionária, o intestino é drenado por duas veias vitalinas (ou onfalomesentéricas). Estas duas veias são ligadas por três ramos: ramo cefálico (localizado no fígado), ramo médio (posterior ao duodeno) e um ramo caudal (anterior ao duodeno). Mais tarde, os ramos caudal e cefálico unem-se à parte caudal da veia vitelina direita. A parte cefálica da veia vitelina esquerda tende a desaparecer. Se os ramos médio e cefálico desaparecerem juntamente com a veia vitelina esquerda, pode ocorrer o surgimento da VPPD3.
A VP drena sangue de todas as partes do aparelho digestivo, pâncreas, baço e vesícula biliar4.
Neste relato de caso, será descrito um recém-nascido diagnosticado com VPPD na Maternidade de Campinas, Campinas-SP.
APRESENTAÇÃO DO CASO
Recém-nascido (RN), sexo feminino, branco, peso de nascimento 1.645 gramas. Idade gestacional pelo método de Capurro compatível com 33 semanas e 1 dia, pequeno para idade gestacional.
Nascido de parto cesárea com bolsa rota de dois dias e oligodramnia grave.
Mãe de 35 anos, quartigesta, realizou cinco consultas de pré-natal, sem intercorrências.
Apresentou desconforto respiratório e apneia na sala de parto, sendo submetido à intubação orotraqueal (IOT).
Nas primeiras 48 horas de vida foi iniciada dieta por gavagem com fórmula infantil. Neste período, apresentou perfusão periférica insatisfatória, necessitando de droga vasoativa (dopamina) por 24 horas.
Já no quarto dia de vida, apresentou distensão abdominal importante, associada a dor, sendo suspensa a dieta por quatro dias para investigação diagnóstica. Permaneceu em nutrição parenteral durante este período, sendo reintroduzida dieta por gavagem.
Recebeu antibioticoterapia com ampicilina e gentamicina por dez dias, por suspeita de infecção ovular. O quadro não apresentou melhora, sendo então optado por oxacilina e amicacina por 5 dias, modificado para piperacilina e tazobactam por mais dez dias.
Apresentou vários episódios de vômitos, em torno do 20º dia de vida. Optou-se pelo início de domperidona, entretanto, sem melhora.
Aos 30 dias de vida, recebeu alta para a Unidade de Cuidados Intensivos (UCI), com peso de 2.195g. Permaneceu internado para investigação de refluxo gastroesofágico (DRGE).
Exames complementares
• Três dias de vida -Ecocardiograma: forame oval pérvio (FOP) 1,2 mm, hipertensão pulmonar (HP) leve 42 mmHg, estenose fisiológica de ramos pulmonares.
• Quarenta e quatro dias de vida - Esôfago Estômago Duodeno (EED): durante deglutição evidenciado refluxo faringo-nasal. Na deglutição em decúbito dorsal evidenciada aspiração do contraste. EED com relevografia de estômago e duodeno e motilidade preservadas. Negativo para pesquisa de DRGE.
• RX tardio de 24 horas, com contraste - suspeita de ceco móvel ao nível do ângulo hepático.
• Quarenta e oito dias de vida - hemoculturas (duas amostras) negativas.
Mesmo após medidas de suporte, paciente permaneceu apresentando episódios de vômitos.
Submetido a procedimento cirúrgico aos 60 dias de vida, para realização de cirurgia de Nissen para correção de doença do refluxo gastroesofágico. Entretanto, no ato cirúrgico foi diagnosticado quadro de veia porta pré-duodenal (Figura 1), sendo realizada correção por duodeno-duodeno anastomose (conforme Figuras 2 e 3) sobre a veia porta anômala pré-duodenal.
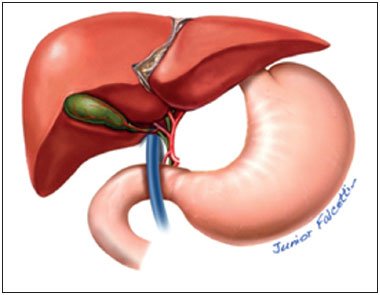
Figura 1. Veia porta pré-duodenal.

Figura 2. Duodeno-duodeno anastomose.
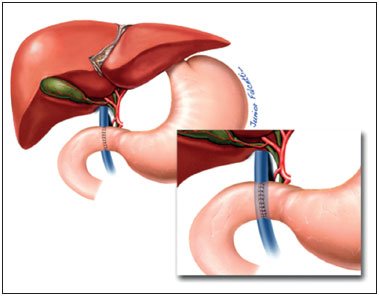
Figura 3. Duodeno-duodeno anastomose.
Encaminhada à UTI neonatal no pós-operatório imediato. Submetida à extubação orotraqueal no dia seguinte à cirurgia, permanecendo em O2 circulante por 2 dias. Manteve bom padrão respiratório, sem sinais de desconforto e bons níveis de saturação de O2, possibilitando permanência em ar ambiente.
Permaneceu sete dias em nutrição parenteral, sendo iniciada dieta com fórmula infantil por gavagem e após sete dias modificada para via oral associada ao leite materno. Apresentou boa aceitação e retenção, sendo solucionados os episódios de vômitos.
No pós-operatório, não recebeu antibioticoterapia por exames seriados de triagem sem alterações. Não necessitou suporte vasoativo. Recebeu analgesia por cinco dias.
Duas semanas após o ato operatório, recebe alta da UTI para UCI.
Permaneceu em UCI por mais seis dias, tendo o quadro completamente solucionado. Recebe alta em uso de bromoprida e ranitidina, pesando 2.270g.
Paciente encontra-se em acompanhamento ambulatorial com equipe da cirurgia pediátrica, recebendo fórmula infantil (por opção da família). Mantém ausência dos episódios de vômitos e apresenta um bom ganho de peso e condições clínicas satisfatórias.
DISCUSSÃO
A VPPD geralmente está associada com má rotação intestinal, situs inversus, atresia duodenal, pâncreas anular, malformações das vias biliares5, anomalias cardíacas e anomalias esplênicas6. Dentre as malformações, destacam-se má rotação intestinal em 64% dos pacientes, situs inversus em 26%, anomalias do duodeno e pâncreas em 26% e 22%, respectivamente1.
A variação da arquitetura portal foi encontrada em 20-35% dos indivíduos7. As duas variações mais comuns incluem: (a) trifurcação da veia porta, na qual há ausência do tronco direito e dos ramos anterior e posterior direito que derivam do mesmo ponto que a veia porta esquerda; e (b) o ramo posterior direito saindo do ramo principal da veia porta, e não a partir do ramo portal direito8. Também já foi descrito dois ramos segmentares individuais fora do seu ponto de origem (Figura 4) 7.

Figura 4. Anatomia normal da veia porta e principais variações anatômicas. A - Anatomia normal da veia porta; B - Trifurcação da veia porta (Cheng tipo II); C - Ramificação precoce do ramo direito posterior para o lobo direito (Cheng tipo III). VP - veia porta; RE - ramo esquerdo da veia porta; RD - ramo direito da veia porta; RDP - ramo direito posterior; RDA - ramo direito anterior.
Cinquenta porcento dos casos de VPPD são sintomáticos. Na maior parte, são descobertos ao acaso durante a laparotomia exploradora3.
Apenas em pequena parte dos casos a obstrução duodenal foi causada por VPPD isoladamente9. Na maioria dos casos, a obstrução foi causada por anomalias associadas, como pâncreas anular e má rotação intestinal1.
O diagnóstico pré-natal ou identificação pré-operatória de VPPD raramente é feito1.
É importante descartar qualquer causa intrínseca ou extrínseca de obstrução duodenal antes de atribuir a VPPD como causa principal da obstrução6. O tratamento de escolha de obstrução duodenal causada pela VPPD é a duodenoduodeno anastomose ou gastro-duodeno anastomose3.
CONCLUSÃO
Existem poucos relatos sobre a formação anômala da veia porta. Necessitam-se de novos estudos e descrições de casos a respeito.
O caso relatado demonstrou, conforme a literatura, a dificuldade do diagnóstico nesse tipo de doença. Neste caso, a única suspeita levantada pelos exames diagnósticos de imagem foi um RX tardio; exame contrastado de EED que mostrou o ceco localizado anormalmente na região epigástrica, no exame inicial contrastado do duodeno não foi notada nenhuma dilatação do mesmo.
Acreditamos que essa doença, assim como outras doenças raras intestinais, como a má rotação in\testinal, necessita de um alto grau de suspeita por parte do pediatra e cirurgião.
Nenhuma criança com suspeita de vômitos e/ou distensão abdominal de origem por má formação deveria receber alta sem investigação. Acreditamos que ganhamos experiência nesse tipo de doença no recém-nascido.
Agradecimentos
Desenhos feitos por Junior Falcetti. São Paulo, 2013.
REFERÊNCIAS
1. Eltayeb AA. Preduodenal portal vein: a cause of duodenal obstruction in one case and incidental finding in another. Surg Curr Res. 2012;2(2):1-3. DOI: http://dx.doi.org/10.4172/2161-1076.1000109
2. Mattox KL, Townsend CM, Beauchamp RD. Sabiston Tratado de Cirurgia: a base biológica da prática cirúrgica moderna. 18a ed. Rio de Janeiro: Elsevier; 2010.
3. Mordehai J, Cohen Z, Kurzbart E, Mares AJ. Preduodenal portal vein causing duodenal obstruction associated with situs inversus, intestinal malrotation, and polysplenia: A case report. J Pediatr Surg. 2002;37(4):E5. PMID: 11912540 DOI: http://dx.doi.org/10.1053/jpsu.2002.31643
4. Keith LM, Arthur FD. Anatomia Orientada para a Clínica. 5a ed. Rio de Janeiro: Guanabara Koogan; 2007.
5. Choi SO, Park WH. Preduodenal portal vein: a cause of prenatally diagnosed duodenal obstruction. J Pediatr Surg. 1995;30(10):1521-2. DOI: http://dx.doi.org/10.1016/0022-3468(95)90430-1
6. Singal AK, Ramu C, Paul S, Matthai J. Preduodenal portal vein in association with midgut malrotation and duodenal web-triple anomaly? J Pediatr Surg. 2009;44(2):e5-7. DOI: http://dx.doi.org/10.1016/j.jpedsurg.2008.10.075
7. Covey AM, Brody LA, Getrajdman GI, Sofocleous CT, Brown KT. Incidence, patterns, and clinical relevance of variant portal vein anatomy. AJR Am J Roentgenol. 2004;183(4):1055-64. PMID: 15385304 DOI: http://dx.doi.org/10.2214/ajr.183.4.1831055
8. Freitas ACT, Godoy JL, Matias JEF, Stadnik LG, Coelho JCU. Comparação entre exames de imagem e achados operatórios em doadores para transplante hepático intervivos. Arq Gastroenterol. 2007;44(4):325-31. DOI: http://dx.doi.org/10.1590/S0004-28032007000400009
9. Esscher T. Preduodenal portal vein-a cause of intestinal obstruction? J Pediatr Surg. 1980;15(5):609-12. DOI: http://dx.doi.org/10.1016/S0022-3468(80)80509-4
1. Médica Residente do Programa de Pediatria do Complexo Hospitalar Ouro Verde (CHOV), Campinas, SP, Brasil - renataalvim@gmail.com. Autora, pesquisadora e redatora do relato de caso
2. Médico Cirurgião Pediátrico da Maternidade de Campinas, SP, Brasil - holimpio@yahoo.com.br. Autor, pesquisador e cirurgião responsável pelo caso
3. Médica Cirurgiã Pediátrica da Maternidade de Campinas, SP, Brasil - marciadovalle@bol.com.br. Autora, pesquisadora e cirurgiã responsável pelo caso
4. Médica Coordenadora da Unidade de Cuidados Intensivos da Maternidade de Campinas, SP, Brasil - monicabarthelson@terra.com.br. Autora, pesquisadora e neonatologista responsável pelo caso
Endereço para correspondência:
Renata Joviano Alvim
COREME Pediatria
Avenida Ruy Rodrigues, nº 3434, Bairro Jardim Yeda
Campinas, SP, Brasil. CEP: 13060-646


