A má-rotação intestinal (MRI) é uma anomalia do intestino médio decorrente de defeitos nas suas etapas embriológicas de herniação, rotação e fixação. Ela pode se apresentar como não rotação, rotação incompleta, rotação reversa e hérnia mesocólica1.
Incide em 0,2-1% da população e é sintomática em 1/2.500-6.000 dos casos2. Em 30-60% dos casos, associa-se a outras malformações e enfermidades como atresia intestinal, divertículo de Meckel, intussuscepção, doença de Hirschsprung, cisto mesentérico, anomalias das vias biliares extra-hepáticas, doença cardíaca congênita, hérnia diafragmática congênita e defeitos de parede abdominal (onfalocele e gastrosquise).
O desenvolvimento embriológico intestinal é complexo. Inicialmente, há herniação intestinal para fora da cavidade abdominal, na qual uma rotação (270°) no sentido anti-horário se faz em relação ao eixo da artéria mesentérica superior. Aproximadamente, na 12a semana de gestação o intestino médio retorna para a cavidade abdominal e a junção duodeno-jejunal (JDJ) se fixa à parede posterior do abdome, na sua porção lateral esquerda da coluna vertebral e ao ligamento de Treitz, enquanto o ceco se fixa no quadrante inferior direito3.
A MRI decorre de falha na rotação intestinal extracelômica, comumente com a JDJ localizada no quadrante superior direito e o ceco no abdome superior. Essa fixação anômala se faz por bandas adesivas na vesícula biliar, duodeno e parede abdominal direita. Como resultado, tem-se uma base mesentérica estreita, o que predispõe ao volvo intestinal. Menos frequentemente, o intestino faz uma rotação (90°) no sentido horário, posicionando o duodeno anteriormente e o cólon posteriormente, com a formação de um túnel que pode obstruir parcialmente os vasos mesentéricos4.
Classicamente, a MRI se manifesta com vômitos biliosos em recém-nascidos. O volvo ocorre na base mesentérica, causando torção dos vasos mesentéricos superiores. A continuidade da isquemia provoca sintomas como hematoquezia, irritabilidade, dor e distensão abdominais. O quadro pode evoluir com necrose intestinal, que se manifesta por eritema abdominal, sinais de peritonite, choque séptico e óbito. Crianças mais velhas podem apresentar volvo crônico, apresentando dor abdominal em cólica, distensão abdominal com vômitos intermitentes, diarreia, sangramento gastrointestinal e desnutrição5.
O diagnóstico pré-natal de MRI isolada é difícil e, geralmente, é feito por observação ultrassonográfica de complicações do volvo (distensão intestinal, peritonite meconial e ascite). Após o nascimento, o sintoma-chave é o vômito bilioso. Em geral, o primeiro exame que se faz é a radiografia simples de abdome, em que se observa sinais de obstrução intestinal e, em casos graves, acompanhada de pneumatose intestinal, o que sugere a hipótese de enterocolite necrosante. Atualmente, o padrão-ouro para o diagnóstico de MRI é a radiografia contrastada gastrointestinal para avaliar a posição da JDJ. Em casos duvidosos, pode-se solicitar radiografias seriadas contrastadas do intestino delgado e enema contrastado para visualização do ceco, cuja posição próxima à JDJ sugere MRI. A ultrassonografia abdominal tem sensibilidade e especificidade inferiores aos exames previamente citados. Nos casos de neonatos com história de vômitos biliosos e quadro de peritonite, após as medidas iniciais, uma laparotomia exploradora pode ser realizada para diagnóstico e tratamento, mesmo sem diagnóstico radiológico4,5.
Ao diagnóstico, em geral, os pacientes necessitam de tratamento cirúrgico com urgência devido ao alto risco da doença. Entretanto, a indicação de tratamento em pacientes assintomáticos permanece controversa5. A correção cirúrgica foi descrita por Ladd, em 1936. O procedimento se baseia na correção anti-horária da rotação do volvo, divisão das faixas de Ladd, alargamento do feixe mesentérico e posicionamento do intestino delgado no quadrante inferior direito e do intestino grosso no superior esquerdo6. A correção laparoscópica foi descrita por Zee e Bax, em 1995, e é semelhante à cirurgia aberta7. A laparoscopia tem sido utilizada em pacientes estáveis, enquanto a técnica aberta é preferida quando há volvo e suas complicações8-10. A apendicectomia cecal, preconizada por muitos autores no tratamento da MRI, é controversa, pois outros a contraindicam9.
RELATO DE CASO
Mãe de 22 anos, com duas gestações e um parto vaginal prévio. Primogênita feminina, saudável e com 5 anos à época da segunda gestação. Realizou pré-natal sem relatos de intercorrências e ultrassonografia obstétrica normal, realizada 5 dias antes do parto. Avô relata que a mãe compareceu ao pronto-socorro em 24/06/2016 devido à perda de líquido transvaginal, com idade gestacional de 26 semanas. Foi feito diagnóstico de amniorrexe prematura, iniciada tocólise e solicitada vaga em unidade de terapia intensiva (UTI) neonatal. Na evolução, constatou-se ausência de batimentos cardíacos fetais e foi diagnosticada morte fetal intrauterina. Assim, foi iniciada indução do parto e a expulsão registrou-se às 11 horas (26/06/2016).
Segundo a mãe, o recém-nascido tinha idade gestacional de 26 semanas, peso de 915 g, sem batimentos cardíacos ou movimentos fetais. Confirmado o óbito, o recém-nascido foi colocado em uma caixa, onde permaneceu por 2 horas. No entanto, a equipe de enfermagem percebeu movimentos respiratórios e acionou a equipe médica, que iniciou manobras de reanimação e de cuidados intensivos. Após reanimação, o recém-nascido foi transferido para o pronto-socorro infantil de um hospital universitário terciário, onde deu entrada às 19 horas (26/06/2016).
À admissão no pronto-socorro, estava em mau estado geral, hipotônico, com as extremidades frias e cianóticas, saturação de oxigênio com 85% em ar ambiente, roncos e crepitações à ausculta pulmonar, frequência cardíaca de 130 bpm, sopro cardíaco, tendo sido feito uso de oxigênio por hood. Foi realizada intubação orotraqueal (IOT) seguida de aspiração e administração de surfactante 200 mg/kg; verificada glicemia capilar (low), prescritos 2 mL de glicose 10%; iniciada antibioticoterapia com ampicilina, sulbactam e gentamicina devido a sepse neonatal precoce e iniciada dobutamina devido a choque distributivo. Foi encaminhado à UTI neonatal.
Exames séricos à admissão: AST = 488,5 U/L, ALT = 89,2 U/L, bilirrubina total = 2,768 mg/dL, indireta = 2,201 mg/dL e direta = 0,567 mg/dL, CK = 443 U/L, CKMB = 426 U/L, hemoglobina = 12,00 g/dL, leucócitos = 28.250/mm³ (2% mielócitos, 6% metamielócitos, 17% bastonetes, 66% segmentados, 1% eosinófilos, 0% basófilos, 23% linfócitos e 10% monócitos), sorologias não reagentes (toxoplasmose, rubéola, sífilis, CMV, HIV, HTLV); hemocultura sem crescimento bacteriano e radiografia de tórax e abdome com discreto infiltrado reticulogranular bilateral e abdome normal Figura 1. Exames posteriores: ecocardiograma (28/06/2016) = PCA de 1,8 mm; ultrassonografia transfontanela (30/06/2016) = dilatação ventricular e ausência de hemorragias.
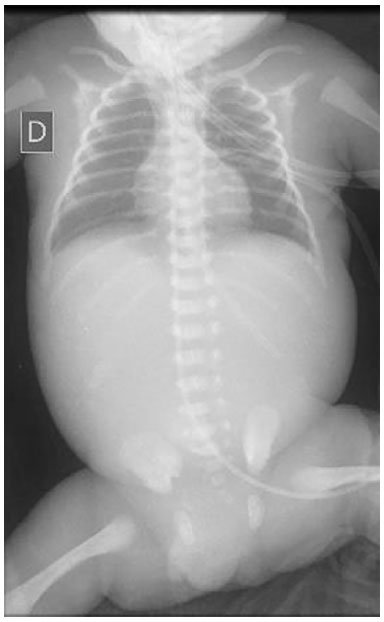 Figura 1. Radiografia simples de tórax e abdome à internação.
Figura 1. Radiografia simples de tórax e abdome à internação.Em 04/07/2016, evoluiu com instabilidade hemodinâmica e distensão abdominal. Radiografia simples de abdome evidenciou obstrução intestinal, pneumoperitônio e sinais de enterocolite necrosante grau III Figura 2. Foi indicada, então, laparotomia exploradora.
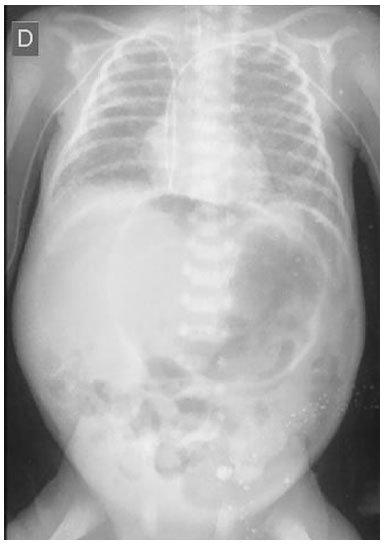 Figura 2. Radiografia simples de abdome no 8º dia de vida: pneumoperitônio (sinal da bola de rugby).
Figura 2. Radiografia simples de abdome no 8º dia de vida: pneumoperitônio (sinal da bola de rugby).O intraoperatório revelou peritonite meconial com perfuração intestinal associada a volvo de intestino médio por MRI a 12 cm da válvula ileocecal e sinais de isquemia, porém, sem necrose. Foi realizada sutura da perfuração, limpeza da cavidade abdominal, exérese de bridas de Ladd entre duodeno e cólon transverso e do ângulo hepático, apendicectomia e reposicionamento das alças intestinais, fechamento dos planos e da incisão transversa supraumbilical à direita Figuras 3 a 6.
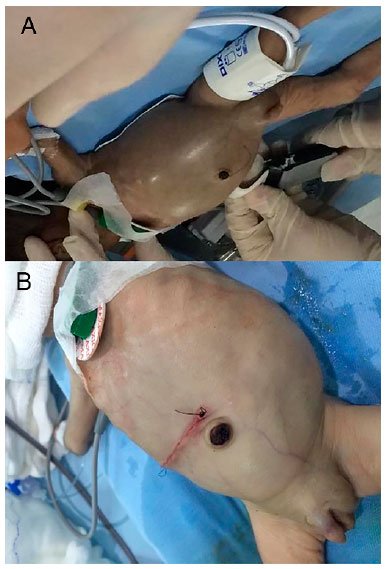 Figura 3. A - Estado do paciente na indução anestésica. Observa-se a discrepância entre as mãos do anestesista e o recém-nascido; B - Estado do paciente no pós-operatório imediato.
Figura 3. A - Estado do paciente na indução anestésica. Observa-se a discrepância entre as mãos do anestesista e o recém-nascido; B - Estado do paciente no pós-operatório imediato.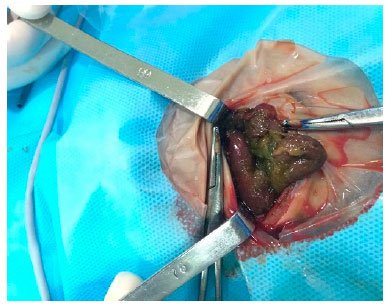 Figura 4. Perfuração intestinal a 12 cm da válvula ileocecal com peritonite meconial.
Figura 4. Perfuração intestinal a 12 cm da válvula ileocecal com peritonite meconial.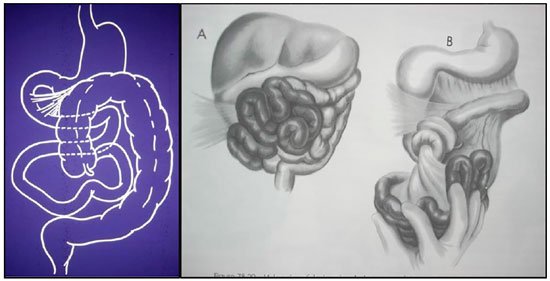 Figura 5. Desenho esquemático do tipo da má-rotação intestinal encontrada seguindo a classificação de Grosfeld (1992).
Figura 5. Desenho esquemático do tipo da má-rotação intestinal encontrada seguindo a classificação de Grosfeld (1992).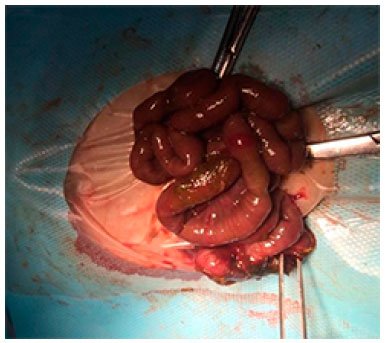 Figura 6. Foto cirúrgica das alças intestinais após sutura da perfuração em íleo terminal e reversão do volvo devido à síndrome da má-rotação intestinal.
Figura 6. Foto cirúrgica das alças intestinais após sutura da perfuração em íleo terminal e reversão do volvo devido à síndrome da má-rotação intestinal.Após recuperação, evoluiu com instabilidade hemodinâmica e distensão abdominal. Outra radiografia simples de abdome evidenciou pneumoperitônio e foi submetido a nova laparotomia (13/07/2016) Figura 7. O intraoperatório revelou duas perfurações, uma a 20 cm do duodeno, próxima ao local de lise de aderências da primeira cirurgia, e outra no local da sutura anterior, que se encontrava bloqueada por alças intestinais. Além disso, havia semioclusão duodenal por resíduo bilioso. Foi realizada sutura da perfuração superior e ressecados 5 cm de alça no local da segunda perfuração, com anastomose terminoterminal. Não havia sinais de peritonite.
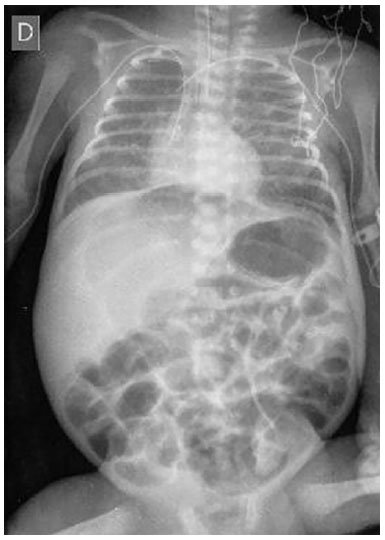 Figura 7. Radiografia simples de abdome para controle no 8º dia de pós-operatório.
Figura 7. Radiografia simples de abdome para controle no 8º dia de pós-operatório.Evoluiu com choque distributivo e distúrbio da coagulação no pós-operatório imediato. Foi diagnosticado com higroma cístico em região parietal em ultrassonografia transfontanela (21/07/2016). Um eletrocardiograma (26/07/2016) evidenciou sobrecarga de câmara direita. Exame de fundo de olho (29/07/2016) revelou retina periférica avascular. Evoluiu com pneumonia associada a broncodisplasia pulmonar (01/08/2016). Necessitou de hemotransfusão devido a anemia (04/08/2016). Foi tentada extubação eletiva (11/08/2016) e mantido em ventilação não invasiva (VNI); porém, evoluiu com apneia, hipotermia e bradicardia, sendo necessária IOT. Com diagnóstico de sepse tardia e hemocultura positiva para Serratia marcescens, recebeu tratamento para pneumonia (16/08/2016). Extubação eletiva (24/08/2016), mantido em VNI, porém com necessidade de reintubação em 25/08/2016, devido a desconforto respiratório e radiografia de tórax evidenciando atelectasia total de pulmão direito.
Apresentou instabilidade hemodinâmica com necessidade de uso de drogas vasoativas e tratamento para sepse com hemocultura positiva para Staphylococcus haemolyticus. Tratamentos para conjuntivite bacteriana (04/09/2016, 19/09/2016 e 15/10/2016). Exame de fundo de olho (09/09/2016) revelou retinopatia da prematuridade estágio 2, zona III, tratada com fotocoagulação a laser (09/09/2016 e 23/09/2016). Extubação eletiva (12/09/2016), com piora do padrão respiratório (21/09/2016) e reintubação. Submetido à herniorrafia bilateral com orquidopexia (22/09/2016). Extubado definitivamente (15/10/2016), manteve bom padrão respiratório em VNI, apesar de estridor respiratório alto e radiografia de tórax com atelectasia à direita. Foi transferido, em 19/10/2016, da UTI para a enfermaria em bom estado geral, respiração espontânea em ar ambiente, peso de 2.310 g e uso de cateter nasogástrico, com boa progressão para dieta via oral.
Novos exames: ecocardiograma (03/10/2016) = FOP de 2,5 mm, PCA de 2,5 mm e fração de ejeção normal; eletroencefalograma (08/11/2016) = atividade epileptiforme em região temporal média à direita e desorganização difusa do traçado. Evoluiu sem intercorrências na enfermaria, foi retirado cateter nasogástrico (10/11/2016) e recebeu alta hospitalar (11/11/2016). No momento do presente relato, encontra-se bem e em seguimento no ambulatório de egressos da UTI.
COMENTÁRIOS
A MRI necessita correção cirúrgica antes da ocorrência do volvo; entretanto, dificilmente o diagnóstico ocorre nesse período. A ultrassonografia abdominal com Doppler viabiliza a localização dos vasos mesentéricos superiores e a verificação da posição da veia em relação à artéria, o que tem demonstrado resultados promissores para o diagnóstico precoce.
REFERÊNCIAS
1. Langer JC. Intestinal rotation abnormalities and midgut volvulus. Surg Clin North Am. 2017; 97:147-59.
2. Ezer SS, Oguzkurt P, Temiz A, Ince E, Gezer HO, Demir S, et al. Intestinal malrotation needs immediate consideration and investigation. Pediatr Int. 2016; 58:1200-4.
3. Morris G, Kennedy A Jr, Cochran W. Small bowel congenital anomalies: a review and update. Curr Gastroenterol Rep. 2016; 18(4):16.
4. Christison-Lagay E, Langer JC. Intestinal rotation abnormalities. Oper Pediatr Surg. 2014; 2:41.
5. Graziano K, Islam S, Dasgupta R. Asymptomatic malrotation: diagnosis and surgical management: an American Pediatric Surgical Association outcomes and evidence based practice committee systematic review. Pediatr Surg. 2015; 50(10):1783-90.
6. Ladd WE. Surgical diseases of the alimentary tract in infants. N Engl J Med. 1936; 215:705-8.
7. van der Zee DC, Bax NM. Laparoscopic repair of acute volvulus in a neonate with malrotation. Surg Endosc. 1995; 9(10):1123-4.
8. Ooms N, Matthyssens LEM, Draaisma JM, et al. Laparoscopic treatment of intestinal malrotation in children. Eur J Pediatr Surg. 2016; 26:376-81.
9. Kinlin C, Shawyer AC. The surgical management of malrotation: A Canadian Association of Pediatric Surgeons survey. J Pediatr Surg. 2017; 52(5):853-8.
10. Ferrero L, Ahmed YB, Philippe P, Reinberg O, Lacreuse I, Schneider A, et al. Intestinal Malrotation and Volvulus in Neonates: Laparoscopy Versus Open Laparotomy. J Laparoendosc Adv Surg Tech A. 2017; 27(3):318-21.
1. Acadêmico de Medicina - Universidade Federal do Triângulo Mineiro - Uberaba - Minas Gerais - Brasil
2. Residente em Medicina Intensiva Pediátrica - Universidade Federal do Triângulo Mineiro - Uberaba - Minas Gerais - Brasil
3. Professora Associada - Universidade Federal do Triângulo Mineiro - Uberaba - Minas Gerais - Brasil
4. Professor Adjunto - Universidade Federal do Triângulo Mineiro - Uberaba - Minas Gerais - Brasil
5. Acadêmica de Medicina - Universidade Federal do Triângulo Mineiro - Uberaba - Minas Gerais - Brasil
Endereço para correspondência:
Antônio Augusto de Andrade Cunha Filho
Universidade Federal do Triângulo Mineiro, Acadêmico de Medicina
Uberaba - Minas Gerais - Brasil. Rua: Frei Paulino, 30 - Nossa Sra. da Abadia
Uberaba - MG, CEP: 38025-180
E-mail: augustoacunha@gmail.com / augustoacunha@hotmail.com
Data de Submissão: 20/05/2018
Data de Aprovação: 07/082018
Recebido em: 20/05/2018


