Origem anômala da artéria coronária esquerda a partir da artéria pulmonar (anomalous left coronary artery from the pulmonary artery - ALCAPA), também conhecida como síndrome de Bland-White-Garland1, é um defeito cardíaco raro, presente em 0,25-0,5% dos pacientes com cardiopatias congênitas, que provoca isquemia do miocárdio, podendo ser progressiva e resultar em cardiomiopatia isquêmica, com insuficiência cardíaca congestiva se manifestando normalmente nos primeiros 2 meses de vida1,2. Pode ocorrer de forma isolada ou estar associada a outros defeitos como ducto arterioso patente, defeito do septo atrioventricular, tetralogia de Fallot e coarctação da aorta1.
A artéria coronária anormal possui uma relativa baixa pressão de perfusão miocárdica e baixo teor de oxigênio decorrente de sua origem na artéria pulmonar. Com a transição para a circulação extrauterina após o nascimento, vasos colaterais sequestram sangue do miorcádio para a artéria pulmonar, levando a um shunt esquerda-direita, isquemia, disfunção miocárdica e, não raro, óbito neonatal2.
O objetivo deste relato é descrever o caso de um lactente masculino, com diagnóstico de ALCAPA, assim como seu desfecho, relacionando-o com a literatura.
RELATO DO CASO
Paciente masculino, 7 meses de idade, com história de déficit pôndero-estatural desde os 5 meses de idade. Em consulta de rotina com o pediatra, foi auscultado ritmo cardíaco irregular, quando então foi suspeitado de cardiopatia. Pais notavam palidez, sudorese intensa e irritabilidade; negavam outros sintomas. A história patológica pregressa não continha informações relevantes – os pais negavam comorbidades, cirurgias prévias, uso de medicações ou internações. Esquema vacinal completo, história alimentar e desenvolvimento neuropsicomotor adequados à idade. Antecedentes obstétricos: mãe GII PI AI, aborto espontâneo no segundo mês de gestação anterior. Mãe realizou 7 consultas de pré-natal com 7 ecografias e uma ecografia morfológica. Paciente nascido a termo, peso adequado à idade gestacional, parto cesárea devido apresentação pélvica, APGAR 10/10. Alta com 48 horas sem intercorrências. A história familiar não revelava algo relevante para o caso em questão.
O exame físico inicial revelou peso de 6.900 g (abaixo do percentil 5 para a idade), FC: 134 bpm, FR: 26 irpm, temperatura: 37,4 ºC, saturação de oxigênio de 96% em ar ambiente, bom estado geral, normocorado, acianótico, hidratado e afebril. Pressão arterial não aferida na primeira avaliação. À ausculta cardíaca, as bulhas cardíacas eram rítmicas e normofonéticas, sem bulhas acessórias, com sopro sistólico de 1+/6+ em área mitral. Fígado palpável a 2 cm do rebordo costal direito. Ausência de edema de membros. Demais aspectos encontravam-se normais.
Foram realizados: radiografia de tórax, que mostrou aumento global da área cardíaca em razão das cavidades esquerdas e pulmões com transparência normal; eletrocardiograma, que evidenciou ritmo sinusal com sobrecarga de ventrículo esquerdo, alterações difusas da repolarização ventricular e onda Q profunda em D1 e AVL; ecocardiograma, que revelou origem anômala da coronária esquerda a partir da pulmonar (coronária direita dilatada), miocardiopatia dilatada, disfunção sistólica moderada do ventrículo esquerdo, câmaras esquerdas aumentadas e insuficiência mitral importante (Figura 1). Exames laboratoriais revelaram anemia hipocrômica e microcítica, leucocitose de 18.839 cél/µL (diferencial sem particularidades) e velocidade de hemossedimentação (VHS) de 18 mm/1 h. A CK-MB apresentou valor normal (18,00 U/L). Demais exames, incluindo contagem de plaquetas, proteína C reativa, enzimas hepáticas, função hepática e renal e eletrólitos, dentro da normalidade.
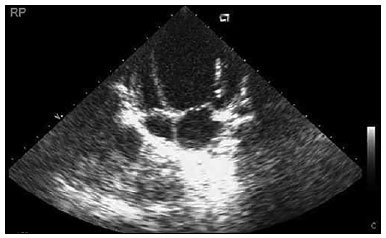 Figura 1. Ecocardiograma bidimensional: miocardiopatia dilatada do ventrículo.
Figura 1. Ecocardiograma bidimensional: miocardiopatia dilatada do ventrículo.Após o diagnóstico ecocardiográfico, foram iniciados carvedilol (0,03 mg/kg/dia), captopril (0,78 mg/kg/dia) e furosemida (1 mg/kg/dia), e solicitado estudo hemodinâmico, que evidenciou origem anômala da artéria coronária esquerda a partir da artéria pulmonar (Figura 2). No 4º dia de hospitalização, foi iniciado digoxina, 0,01 mg/kg/dia, e iniciado preparo de estabilização do paciente, que se encontrava em crise de broncoespasmo, para cirurgia. No 13º dia de hospitalização foi realizado o procedimento de reimplante da artéria coronária esquerda na artéria aorta, com patch de pericárdio autólogo, devido a tronco curto de artéria pulmonar, e plastia de valva mitral. Foi encaminhado à Unidade de Terapia Intensiva Cardíaca para a estabilização pós-cirúrgica. Eletrocardiograma pós-operatório normal e ecocardiograma mostrou insuficiência mitral residual leve, câmaras esquerdas aumentadas, disfunção sistólica leve do ventrículo esquerdo (fração de ejeção de 28%). Evoluiu satisfatoriamente e foi extubado após 5 dias. Recebeu alta para enfermaria após 9 dias de pós-operatório, com prescrição de digoxina, furosemida, enalapril e espironolactona, e evoluiu com melhora progressiva da função cardíaca. Alta hospitalar após 14 dias da cirurgia.
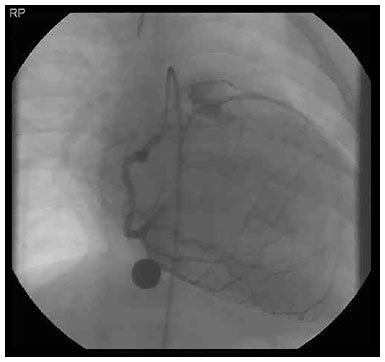 Figura 2. Cateterismo cardíaco evidencia artéria coronária esquerda com origem a partir da artéria pulmonar.
Figura 2. Cateterismo cardíaco evidencia artéria coronária esquerda com origem a partir da artéria pulmonar.A síndrome de ALCAPA (anomalous left coronary artery from the pulmonary artery) é de difícil diagnóstico, e deve ser suspeitada em crianças com miocardiopatia dilatada3. Cerca de 85% dos casos se manifestam até os 2 meses de idade, porém os sintomas podem ser mal interpretados e a doença subdiagnosticada4. Normalmente, o paciente apresenta sinais de choque e o exame físico revela ritmo de galope ou sopro de regurgitação mitral, devido à disfunção do músculo papilar decorrente da isquemia do miocárdio. Um sopro contínuo que sugere persistência do canal arterial, com fluxo da aorta para a artéria pulmonar (shunt esquerda-direita) pode ser indicativo de fluxo pelas artérias colaterais2.
As manifestações clínicas apresentadas pelo nosso paciente, como sudorese, palidez, irritabilidade, choro intenso e baixo ganho ponderal, são as mesmas descritas na literatura, e estão correlacionadas ao shunt esquerda-direita e consequente insuficiência cardíaca por disfunção ventricular, regurgitação mitral, infarto do miocárdio e disritmias malignas1,2,5-7. É importante observar que alguns pacientes apresentam sopro sistólico devido a insuficiência mitral causada por má perfusão valvar, e este achado, como no caso do paciente em questão, pode ser o sinal clínico de suspeição e motivo de encaminhamento para investigação junto ao cardiologista7.
Exames diagnósticos complementares incluem radiografia de tórax, eletrocardiograma, ecocardiograma e cateterismo cardíaco, sendo que o padrão-ouro é a angiografia das coronárias2. Os achados de cardiomegalia e traçado eletrocardiográfico de infarto agudo do miocárdio, com alterações no segmento ST ou onda Q em DI, AVL, V5 e V6, são sugestivos1,8. Em crianças, o diagnóstico normalmente pode ser feito por ecocardiograma bidimensional com visualização direta da origem anormal da artéria coronária esquerda e fluxo retrógrado para a artéria pulmonar, além de regurgitação mitral e aumento da ecogenicidade dos músculos papilares da valva mitral4. Ecocardiograma também é um exame indispensável na avaliação da fração de ejeção, especialmente na evolução pós-operatória9. Outros exames são a angiotomografia e angiorressonância magnética das coronárias, que, na prática, cedem lugar ao estudo hemodinâmico na avaliação do paciente10. Enzimas miocárdicas, como CKMB ou troponina, podem estar aumentadas, porém não têm papel diagnóstico1,10.
A doença requer tratamento cirúrgico que restabeleça o fluxo de sangue oxigenado para o miocárdio. O procedimento de escolha consiste em reimplantar a coronária na aorta9. A plastia da valva mitral pode ser realizada no mesmo tempo cirúrgico, sendo inclusive recomendada, uma vez que o paciente apresenta disfunção valvar2. Outras opções incluem realizar uma tunelização da artéria coronária para a aorta (reparo de Takeuchi) ou, ainda, realizar um bypass aorto-coronário com artéria mamária interna ou veia safena10,11. Estima-se que a mortalidade cirúrgica seja menor que 5-10%. O prognóstico, frequentemente, é excelente após a reimplantação da artéria coronária esquerda anômala10.
No pré-operatório, os pacientes são estabilizados com diuréticos e, eventualmente, com agentes inotrópicos e anti-hipertensivos, além de condutas de rotina como infusão de hemocomponentes, conforme a necessidade clínica5. O manejo pós-operatório deve ser realizado em Unidade de Terapia Intensiva e, em geral, requer agentes inotrópicos, drogas redutoras de pós-carga, diuréticos, além de ventilação mecânica5,10. No pós-operatório intermediário, existe uma tendência à melhora da fração de ejeção, e o paciente pode permanecer com insuficiência mitral residual leve9. O seguimento do paciente deve incluir a avaliação periódica da função ventricular e possível obstrução do reimplante da coronária12.
O quadro clínico de insuficiência cardíaca congestiva nos primeiros 1 a 2 meses de vida com sinais de taquicardia, diaforese e recusa alimentar com baixo ganho ponderal, deve levar à investigação cardiológica. O diagnóstico do paciente em questão se deu de forma tardia, uma vez que a falha no reconhecimento clínico precoce desta condição levou ao atraso na busca ao serviço de referência. Mesmo com o estabelecimento de insuficiência cardíaca, o tratamento do paciente com as técnicas e recomendações empregadas na literatura resultou em um desfecho satisfatório.
REFERÊNCIAS
1. Mancini MC. Anomalous left coronary artery from the pulmonary artery. Medscape [periódicos na Internet]. 2017 Jan. Disponível em: http://emedicine.medscape.com/article/893290-overview. Acesso em: 22 mar 2017
2. Koenig PR, Hijazi ZM, Graham TP, Triedman JK. Congenital and pediatric coronary artery abnormalities. In: UpToDate, Post TW (Ed), UpToDate, Waltham, MA; 2010.
3. Gribaa R, Slim M, Ben Salem H, Neffati E, Boughzela E. Anomalous origin of the left coronary artery from the pulmonary artery presenting as dilated cardiomyopathy: a case report. J Med Case Rep. 2014; 8:170.
4. Kristensen T, Kofoed KF, Helqvist S, Helvind M, Søndergaard L. Anomalous origin of the left coronary artery from the pulmonary artery (ALCAPA) presenting with ventricular fibrillation in an adult: a case report. J Cardiothorac Surg. 2008; 3:33.
5. Younus Z, Iftikhar R, Iftikhar A. Anomalous origin fo left coronary artery from pulmonary artery (ALCAPA). J Coll Physicians Surg Pakistan. 2013; 23(10):743-744.
6. Modi H, Ariyachaipanich A, Dia M. Anomalous origin of right coronary artery from pulmonary artery and severe mitral regurgitation due to myxomatous mitral valve disease: a case report and literature review. J Invasive Cardiol. 2010; 22(4):49-55.
7. Rodriguez-Gonzalez M, Tirado AM, Hosseinpour R, de Soto JS. Anomalous Origin of the left coronary artery from the pulmonary artery: diagnoses and surgical results in 12 pediatric patients. Texas Hear Inst J. 2015; 42(4):350-356.
8. Bakiler AR, Eliaçik K, Köse S AY. Anomalous origin of the left coronary artery from the pulmonary artery presenting as dilated cardiomyopathy. Arch Turk Soc Cardiol. 2013; 41(5):448-450.
9. Muzaffar T, Ahmad Ganie F, Gpoal Swamy S, Wani N-U-D. The surgical outcome of anomalous origin of the left coronary artery from the pulmonary artery. Int Cardiovasc Res J. 2014; 8(2):57-60.
10. Mancini MC. Surgical Approach to Anomalous Left Coronary Artery From the Pulmonary Artery. Medscape. 2015 May. Disponível em: http://emedicine.medscape.com/article/905229-overview. Acesso em: 05 abril 2017
11. Lenzi AW, Solarewicz L, Ferreira WS, Sallum F, Miyague NI. Análise da técnica de Takeuchi usada para o tratamento da origem anômala da artéria coronária esquerda do tronco pulmonar. Arq Bras Cardiol. 2008; 90(3):185-190.
12. Yuan S-M. Anomalous origin of coronary artery: taxonomy and clinical implication. Braz J Cardiovasc Surg. 2014; 29(4):622-629.
1. Médica-Residente em Pediatria
2. Acadêmico de Medicina
3. Doutora em Saúde da Criança e Adolescente. Médica Cardiologista Pediátrica e Ecocardiografista
Endereço para correspondência:
Angélica Luciana Nau
Hospital Pequeno Príncipe
Desembargador Motta, 1070
Água Verde, Curitiba, Paraná, Brasil. - CEP 80250-060
Data de Submissão: 18/06/2017
Data de Aprovação: 16/10/2017
Recebido em: 18/06/2017
Aceito em: 16/10/2017


